
Weitreichendes Off-Label-Potenzial: Erdafitinib als Option für zahlreiche Tumortypen
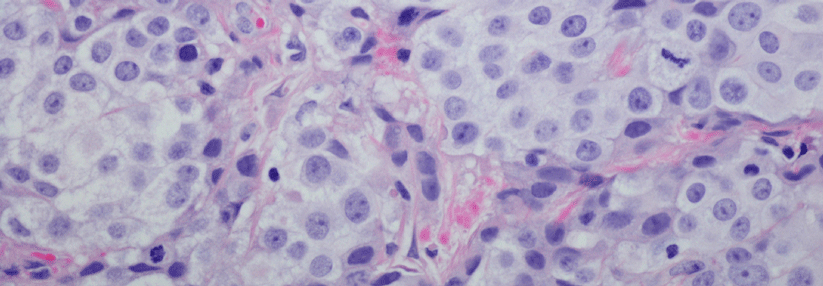 Die FDA gab im März 2019 die Zulassung zur Behandlung des fortgeschrittenen Urothelkarzinoms.
© iStock/OGphoto
Die FDA gab im März 2019 die Zulassung zur Behandlung des fortgeschrittenen Urothelkarzinoms.
© iStock/OGphoto
Im März 2019 gab die FDA in einem beschleunigten Verfahren Erdafitinib die Zulassung zur Behandlung des fortgeschrittenen Urothelkarzinoms. Voraussetzung für den Einsatz sind Genalterationen der Rezeptoren FGFR2/3. Basis dieser Entscheidung war eine Phase-2-Studie, in der je nach Art der vorliegenden Mutation im FGFR2- oder FGFR3-Gen Ansprechraten zwischen 0 und 40,6 % auftraten – mit einer medianen Ansprechdauer von 5,4 Monaten.
Neben dem Urothelkarzinom finden sich solche Veränderungen u.a. häufig auch bei Tumoren von Brust, Endometrium, Pankreas, Kolon, Rektum und nicht-kleinzelligem Lungenkrebs. Der Enthusiasmus für derartige Präzisionstherapien ist groß. In einem…
Bitte geben Sie Ihren Benutzernamen und Ihr Passwort ein, um sich an der Website anzumelden.
