Neue Wirkstoffe beim hereditären Angioödem sind in der Entwicklung
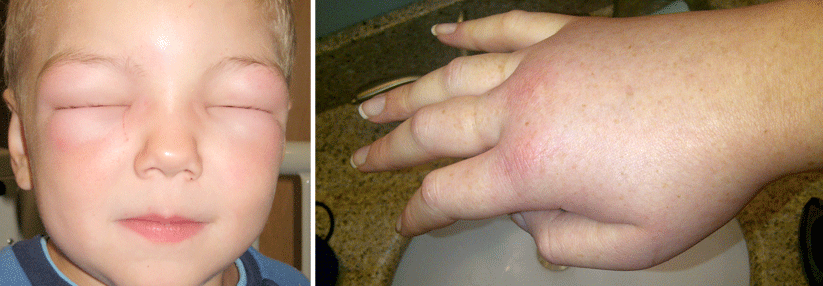
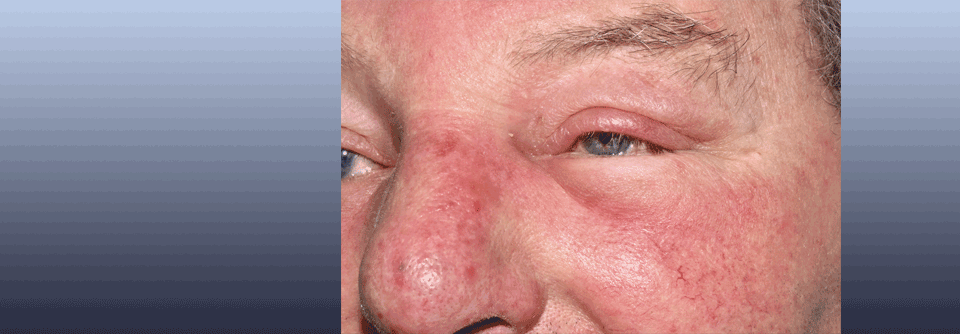
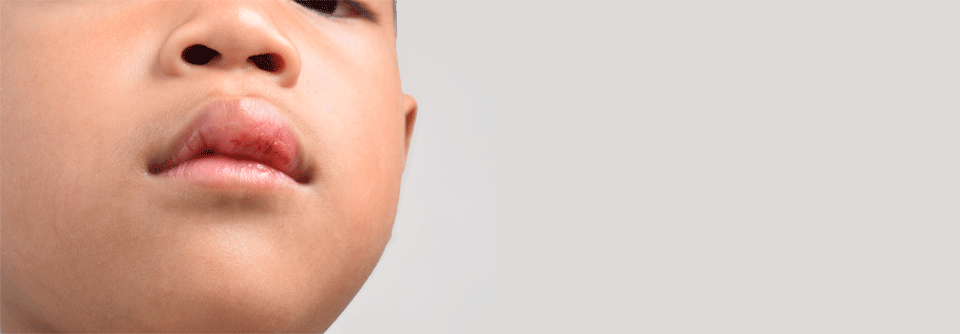 Ödeme im Gesicht, Schwellungen im GI-Trakt und krampfartige Bauchschmerzen – die Lebensqualität von Menschen mit hereditärem Angioödem ist stark eingeschränkt.
© Mulad Images - stock.adobe.com
Ödeme im Gesicht, Schwellungen im GI-Trakt und krampfartige Bauchschmerzen – die Lebensqualität von Menschen mit hereditärem Angioödem ist stark eingeschränkt.
© Mulad Images - stock.adobe.com
Das hereditäre Angioödem (HAE) ist eine autosomal-dominante Erkrankung mit einer Prävalenz von ca. 1/50.000. Somit handelt es sich zwar um eine seltene Erkrankung, dennoch wurden im vergangenen Jahr gleich mehrere relevante Studien publiziert, berichtete Prof. Dr. Carsten Schmidt vom Klinikum Fulda. Ursächlich ausgelöst wird das HAE entweder durch einen Mangel (HAE Typ 1) oder eine verminderte Aktivität (HAE Typ 2) des Enzyms C1-Esterase-Inhibitor. Aufgrund des einen oder anderen Defizits entfällt die Hemmung des Kallikrein-Kinin-Systems und es wird vermehrt Bradykinin ausgeschüttet.
Das wiederum führt zu lokalen Schwellungen und ausgeprägten Ödemen im Bereich der Haut – vor allem am Stamm, an den Extremitäten und im Gesicht. Darüber hinaus ist bei fast allen Patientinnen und Patienten der Gastrointestinaltrakt von Schwellungen der Submukosa betroffen. Diese können zu Obstruktionen und sehr starken abdominellen Schmerzen führen. Nicht zuletzt können die Schwellungen auch im Bereich des Larynx auftreten und somit lebensbedrohlich werden.
Über die Bestimmung der C1-Esterase-Inhibitor-Konzentration und die Messung von dessen Aktivität kann die Krankheit recht einfach diagnostiziert werden. Die C4-Konzentration ist bei beiden HAE-Formen reduziert. Es gibt bereits einige Behandlungsoptionen, die sowohl zur Prophylaxe als auch zur Akuttherapie der Schübe zur Verfügung stehen. Im letzten Jahr wurden durch zwei neue Publikationen weitere Kandidaten ins Visier genommen.
Symptome klangen innerhalb von knapp acht Stunden ab
So konnte in einer randomisierten placebokontrollierten Studie gezeigt werden, dass der Plasma-Kallikrein-Inhibitor Sebetralstat eine schnelle und effektive Symptomlinderung bei HAE-Attacken bewirkt, und zwar unabhängig von deren Schwere.1 Während die Schubsymptomatik unter Placebo mehr als zwölf Stunden anhielt, klang sie unter 600 mg Sebetralstat innerhalb von 7,75 Stunden ab.
Eine Prophylaxe der HAE-Attacken gelingt laut einer weiteren Studie mit der subkutanen Gabe von Donidalorsen, einem RNA-gerichteten Wirkstoff. Vor allem unter dem Regime, bei dem alle vier Wochen eine Applikation erfolgte, reduzierte er die Schubrate deutlich.2 Auch die Lebensqualität, die unter HAE stark eingeschränkt ist, verbesserte sich durch die Donidalorsengabe. Die Marktzulassung wurde vom Hersteller beantragt.
Prof. Schmidt hob eine aktuell publizierte Phase-2-Studie besonders hervor: In einer der ersten klinischen Anwendungen wurde die sogenannte Genschere CRISPR* eingesetzt, um das Gen KLKB1, welches das Protein Kallikrein kodiert, zu bearbeiten. Ziel war es, mit einer einmaligen oralen Gentherapie eine lebenslange Kontrolle der Erkrankung zu erreichen. Eine kleines Patientenkollektiv wurde 2:2:1 randomisiert. Eine Gruppe erhielt die CRISPR-basierte Therapie NTLA-2002 in einer einmaligen Dosis von 50 mg, die zweite Gruppe bekam eine reduzierte Dosis mit 25 mg. Den Kontrollpersonen wurde ein Placebo verabreicht.
Der primäre Endpunkt war die Anzahl der monatlichen Attacken während der ersten 16 Wochen. Diese ging unter der Behandlung mit NTLA-2002 deutlich zurück. Während die Teilnehmenden vor der Therapie im Schnitt etwa 3,7 HAE-Schübe pro Monat erlitten, waren es danach 0,62 Attacken (unter 50 mg) bzw. 0,7 (unter 25 mg). In der Placebogruppe kam es im Mittel zu 2,82 monatlichen Attacken. Das entsprach einer relativen Reduktion der HAE-Schübe um 77 % bzw. 75 %. Die Studie konnte außerdem zeigen, dass der Therapieeffekt trotz nur einmaliger Gabe in der Verumgruppe sehr langanhaltend war. Er wurde über fast ein Jahr beobachtet.
Nebenwirkungen wie Schwindel fielen mild aus
Bei acht von elf Teilnehmenden aus der Gruppe mit der höheren Dosierung kam es über den gleichen Zeitraum zu keiner einzigen Attacke. Dies gelang mit dem niedrig dosierten Medikament etwas seltener (vier von zehn Behandelten) und gar nicht bei den Personen, die ein Scheinmedikament erhalten hatten. Prof. Schmidt berichtete, dass die Kallikrein-Plasmakonzentrationen unter der Behandlung sehr frühzeitig und nachhaltig abfielen. Es traten lediglich milde Nebenwirkungen auf (Kopfschmerzen, Schwindel, Fatigue).
„Es handelt sich um eine sehr vielversprechende Therapie mit einem ganz neuen Ansatz“, so der Experte. Man könne deshalb gespannt sein auf die Ergebnisse der Phase-3-Studie, die seit Januar läuft. „Für uns ist es wichtig, dass wir hin und wieder an diese Erkrankung denken sollten“, resümierte Prof. Schmidt.
*Clustered Regularly Interspaced Short Palindromic Repeats
Quelle: 1.Riedl MA et al. N Engl J Med 2024; 391: 32-43;
doi: 10.1056/NEJMoa2314192
2.Riedl MA et al. N Engl J Med 2024; 391: 21-31;
doi: 10.1056/NEJMoa2402478
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).