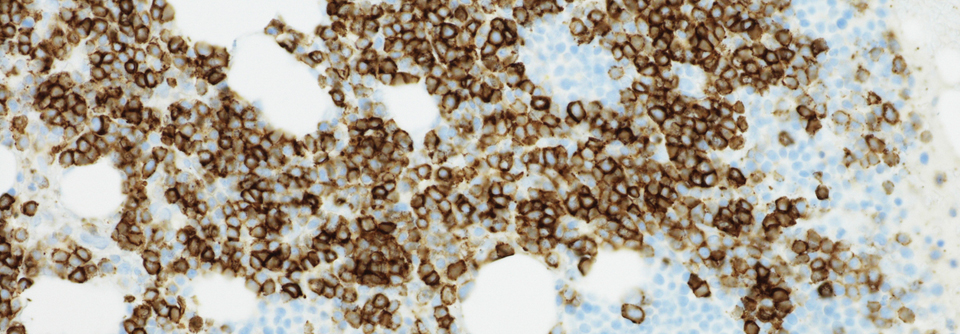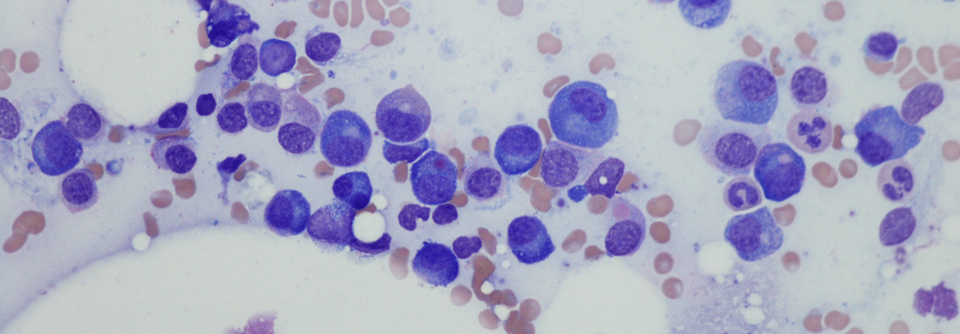
Verschiedene Konzepte können die Progression zum Multiplen Myelom bremsen
 Genetische Veränderungen und der 20-2-20-Risikoscore helfen, das Fortschreiten von Smouldering Myelom vorherzusagen.
© luchschenF – stock.adobe.com
Genetische Veränderungen und der 20-2-20-Risikoscore helfen, das Fortschreiten von Smouldering Myelom vorherzusagen.
© luchschenF – stock.adobe.com
Das Progressionsrisiko eines Smouldering Myeloms (SMM) zu einem Multiplem Myelom lässt sich abschätzen, informierte Prof. Dr. Kwee Yong, University College London Hospitals, NHS Foundation Trust, London. Und zwar unter anderem mit dem 20-2-20-Risikoscore, der folgende Parameter beinhaltet:
- das Verhältnis der freien Leichtketten > 20,
- das Serum-Spike-Protein > 2 g/dl und
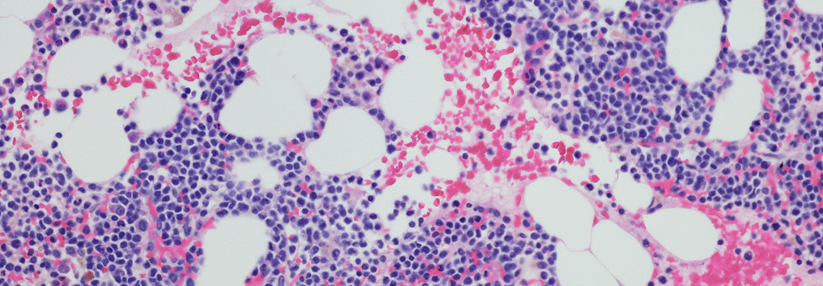
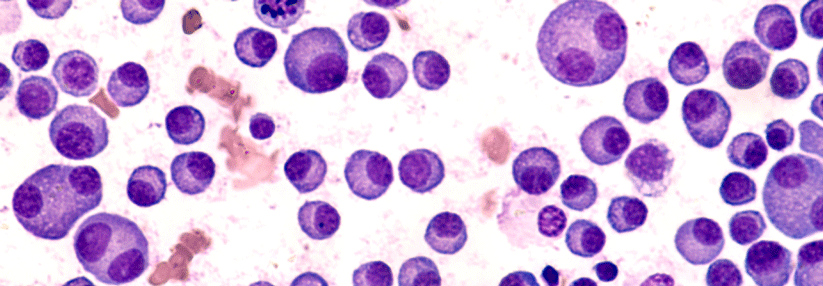
- Plasmazellen im Knochenmark > 20 %.
Liegt keiner dieser Risikofaktoren vor, beträgt die Wahrscheinlichkeit für eine Progression nach zwei Jahren 5 %. Ist einer der Parameter gegeben, sind es 17 % und bei zwei oder drei Faktoren 46 %. Jeweils rund ein Drittel der Patient:innen fällt in eine der drei Risikogruppen, so die Kollegin.
Auch mittels genetischer Alterationen lasse sich das Progressionsrisiko bestimmen. Der relativ neu etablierte MM-like-Score bezieht 26 genetische Myelom-Treiber ein. Zwei davon – t(14;16) und t(14;20) – treten signifikant häufiger auf bei Personen mit SMM/ monoklonaler Gammopathie unklarer Signifikanz (MGUS), während 24 andere, u. a. NRAS, MYC und KRAS, vor allem beim Multiplen Myelom zu finden sind. Der MM-like-Score errechnet sich aus der Anzahl der Myelom-Treiber minus der Anzahl der MGUS/SMM-Treiber. Er unterscheidet nicht nur die Vorläufererkrankungen vom Multiplen Myelom, sondern auch Personen mit niedrigem, intermediärem und hohem Risiko.
Was wollen die Patient:innen?
Im Fall einer asymptomatischen Erkrankung wie dem SMM sei die Perspektive der Betroffenen besonders wichtig, so Prof. Yong. „Wir müssen verstehen, was den Patient:innen am wichtigsten ist. Was sind ihre Prioritäten, wollen sie eine Therapie und was sind ihre größten Bedenken?“ Auch müsse man sich fragen, warum sich die Erkrankten für den einen oder den anderen Weg entscheiden.
Intensive Konzepte mit Chance auf Heilung
Die Frage sei, ob man die Malignome bereits im Vorläuferstadium erfolgreich bekämpfen kann, bevor sie sich zu einer genomisch fortgeschrittenen Erkrankung entwickeln. Forschende prüfen dazu verschiedene intensive Strategien. „Die Patient:innen sind allerdings meist älter und gebrechlich, deshalb eignen sich wahrscheinlich nicht viele dafür“, erläuterte Prof. Yong. Mit den Ansätzen würden aber hohe und tiefe Ansprechraten erzielt, was auf eine mögliche Heilung hindeutet.
Als Beispiel nannte die Referentin die Kombination aus Carfilzomib, Lenalidomid und Dexamethason (KRd), gefolgt von einer Transplantation, KRd-Konsolidierung und Lenalidomid-Dexamethason-Erhaltung. Das Ergebnis: Selbst Personen, die am Ende der Erhaltungstherapie MRD-negativ waren, erlitten teilweise einen Progress – allerdings weniger häufig als die MRD-positiven Teilnehmenden.
Ein weiteres Konzept beruht darauf, das Fortschreiten durch eine Immunmodulation zu verhindern. Das Sicherheitsprofil scheine besser zu sein und die Strategie könne bei insgesamt mehr Personen zum Einsatz kommen. Aber: Sie vernichtet den Klon nicht und das Ansprechen fällt insgesamt geringer aus. Die Kombination aus Lenalidomid und Dexamethason sei eine solche Strategie, die gegenüber keiner Therapie sowohl die Zeit bis zur Progression zu einem Multiplen Myelom als auch das Gesamtüberleben verlängerte.
Daratumumab versus aktive Überwachung
Erst kürzlich wurde die Phase-3-Studie AQUILA präsentiert, in der SMM-Patient:innen mit teils hohem Risiko entweder den CD38-Antikörper Daratumumab für drei Jahre erhielten oder aktiv überwacht wurden. Nach einem medianen Follow-up von 65,2 Monaten war das mediane PFS im Prüfarm nicht erreicht vs. 41,5 Monate in der Kontrolle. Das Fünf-Jahres-PFS erreichte 63,1 % vs. 40,8 % (HR 0,49; p < 0,001), das Fünf-Jahres-OS 93 % vs. 86,9 % (HR 0,52). Auf Daratumumab sprachen 63,4 % an, davon nur 8,8 % mit einer mindestens kompletten Remission. „Es handelt sich hierbei aber nicht um eine kurative Strategie“, erläuterte die Expertin.
In der ImmunoPRISM-Studie erhielten Personen mit Hochrisiko-SMM u. a. Teclistamab. Alle erzielten durch die Therapie eine MRD-Negativität, 83 % sprachen komplett auf das Bispezifikum an. Nach fünf Monaten kam es zu einer klonalen Expansion von T-Zellen, insbesondere von CD8+ zytotoxischen Effektor-Gedächtniszellen.
Auf die Frage, ob Prof. Yong Hochrisiko-SMM-Erkrankte außerhalb von klinischen Studien behandeln würde, antwortete sie: „Zum jetzigen Zeitpunkt würde ich eine Therapie außerhalb klinischer Studien nicht empfehlen. Wir haben bisher noch nicht genügend Informationen oder Tools an der Hand, um zu entscheiden, wen wir mit was behandeln sollten.“
Quelle:
Yong K. EHA2025; Vortrag: „Updates on smoldering multiple myeloma“
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).