Wie sich die Behandlung verändern wird
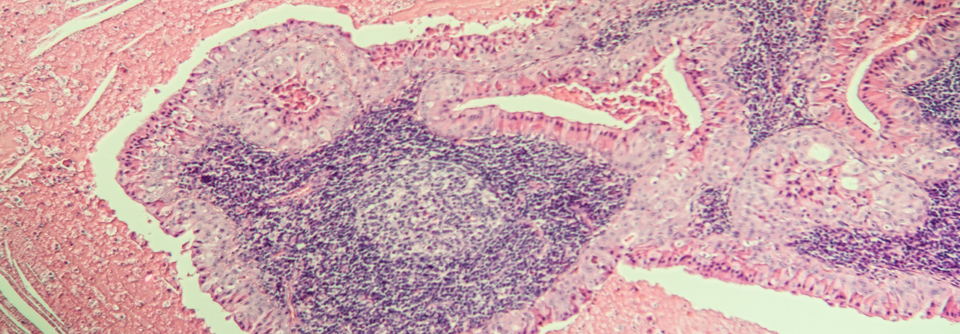
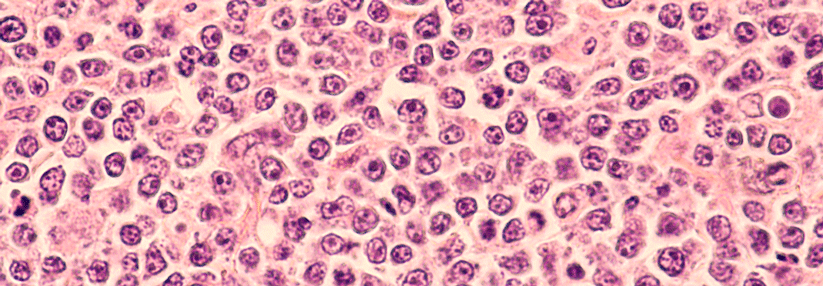
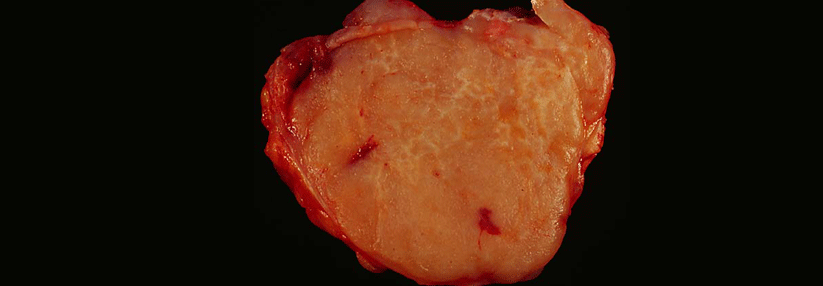
 Patient:innen mit kutanen T-Zell-Lymphomen können auf Fortschritte durch neue zielgerichtete Substanzen und Kombinationstherapien hoffen.
© Irene – stock.adobe.com
Patient:innen mit kutanen T-Zell-Lymphomen können auf Fortschritte durch neue zielgerichtete Substanzen und Kombinationstherapien hoffen.
© Irene – stock.adobe.com
Seitdem 2018 Brentuximab-Vedotin (BV) für die Therapie CD30+ kutaner T-Zell-Lymphome (CTCL) und Mogamulizumab für die rezidivierte oder refraktäre (r/r) Mycosis fungoides und das Sézary-Syndrom zugelassen wurden, gab es keine Neuzulassungen für diese Tumorentität. Wie Prof. Dr. Chalid Assaf, Helios-Klinikum Krefeld, betonte, seien aber innovative zielgerichtete Therapien und Kombinationen unterwegs.1
So habe Mogamulizumab plus extrakorporale Photopherese in einer kleinen Studie bei Erkrankten mit fortgeschrittenen CTCL vielversprechende Ergebnisse erzielt. Die Verträglichkeit war gut. Derzeit würden auch Kombinationen von Mogamulizumab mit einer hypofraktionierten, niedrig dosierten Ganzhaut-Elektronenstrahltherapie (LD-TSEBT) sowie Substanzen wie BV, Checkpoint-Inhibitoren oder der Anti-CD47-Antikörper Magrolimab geprüft.
In der Pipeline stehe auch die Evaluation von BV zusammen mit einer ultra-hypofraktionierten TSEBT („Krefeld-Schema“) bei fortgeschrittenen CTCL. Die Kombi habe zu nahezu vollständigen Remissionen geführt, berichtete Prof. Assaf. Die Gesamtansprechrate (ORR) betrug 100 %, mit 64 % kompletten Remissionen.
Daneben testen Forschende zielgerichtete Substanzen mit neuen Targets, die zunehmend an biologischen Parametern ausgerichtet werden, berichtete Prof. Dr. Pietro Quaglino, Universität Turin.2 Die experimentellen Therapien adressierten drei Kategorien von Molekülen:
- Zielstrukturen wichtiger Signalwege wie TCR/CD28 oder JAK/STAT
- Immunologisch bedeutsame Targets wie PD1 oder CD47
- Oberflächenmoleküle wie CCR4, CD30, CD25, CD70, CD37, TRBC1/1 oder KIR3DL2
Beispielhaft für die erste Gruppe nannte Prof. Quaglino den JAK-Inhibitor Ruxolitinib zur Behandlung des r/r CTCL. In einer Studie mit 48 Betroffenen sei eine ORR von 23 % mit 6 % kompletten Remissionen erreicht worden. Dabei sprachen die Kohorten mit aktivierender JAK/STAT-Mutation oder mit ≥ 30 % immunhistochemisch bestimmter pSTAT-Expression ohne aktivierende JAK/STAT-Mutation am besten an (ORR 28 % bzw. 31 %).
Zulassung in Aussicht
Resminostat erhielt 2023 von der EMA die „Orphan Drug Designation“; aktuell läuft das Zulassungsverfahren in der EU.
Neue Therapieansätze beim CTCL
Exemplarisch für die zweite Gruppe präsentierte der Referent eine Phase-2-Studie. Darin erhielten Patient:innen mit r/r CTCL den PD-L1-Inhibitor Durvalumab zusammen mit Lenalidomid oder alleiniges Durvalumab. Mit der Kombination wurde in einer frühen Auswertung eine ORR von 58 % erreicht vs. 36 % in der Kontrolle. Zur dritten Gruppe gehört der Anti-KIR3DL2-Antikörper IPH4102, der in vorläufigen Untersuchungen beim fortgeschrittenen CTCL eine ORR von 44 % erzielte, beim Sézary-Syndrom sogar von 50 %.
Weiter fortgeschritten ist die Prüfung von Resminostat, einem oral verabreichten Histon-Deacetylase-Inhibitor der Klassen I, IIb und IV. Die Substanz wird als Erhaltungstherapie nach mindestens erreichter Krankheitsstabilisierung durch die Vortherapie eingesetzt. In der Phase-2-Studie RESMAIN wurde laut Prof. Quaglino eine Verdopplung des medianen progressionsfreien Überlebens (8,3 Monate vs. 4,2 Monate) sowie der medianen Zeit bis zur nächsten Behandlung (8,8 Monate vs. 4,2 Monate) im Vergleich zu Placebo erzielt. Das Gesamt-PFS, das auch die Vortherapie einschließt, verbesserte sich auf 24,3 Monate vs. 14,9 Monate.
Quellen:
1. Assaf C. 21st EADO Congress; Vortrag „Recently approved treatment approaches“
2. Quaglino P. 21st EADO Congress; Vortrag „Products under current clinical developments“
Falls Sie diesen Medizin Cartoon gerne für Ihr nicht-kommerzielles Projekt oder Ihre Arzt-Homepage nutzen möchten, ist dies möglich: Bitte nennen Sie hierzu jeweils als Copyright den Namen des jeweiligen Cartoonisten, sowie die „MedTriX GmbH“ als Quelle und verlinken Sie zu unserer Seite https://www.medical-tribune.de oder direkt zum Cartoon auf dieser Seite. Bei weiteren Fragen, melden Sie sich gerne bei uns (Kontakt).