Kardiale Bildgebung Gut deformiert: ein Überblick über den myokardialen Strain
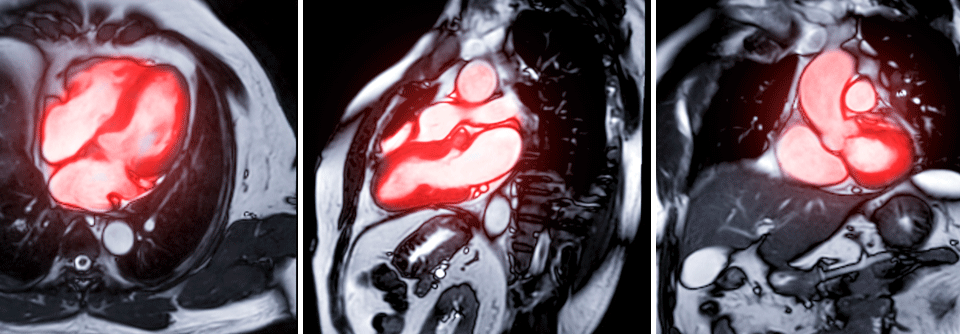
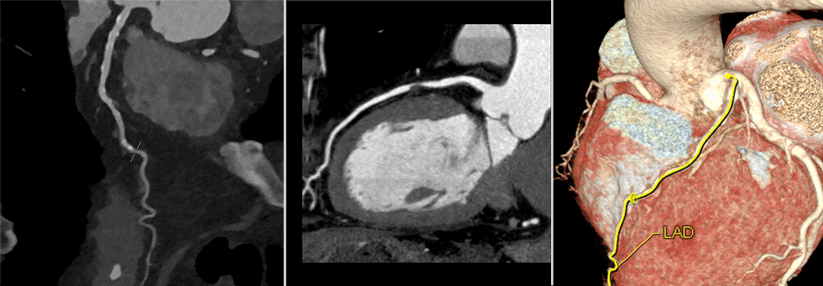
 Der myokardiale Strain lässt sich via Echo, MRT oder CT ermitteln.
© iStock/Nitchawat_Paiyabhroma
Der myokardiale Strain lässt sich via Echo, MRT oder CT ermitteln.
© iStock/Nitchawat_Paiyabhroma
Vor drei Jahren beschrieb die Heart Failure Association der ESC* in einem Positionspapier einen Paradigmenwechsel. Damit meinte sie nicht das Potenzial neuer Herzinsuffizenz-Medikamente, sondern den Wandel in der kardialen Bildgebung. Ein Parameter, der immer wichtiger wird, ist der myokardiale Strain, definiert als das Ausmaß der Verkürzung bzw. Verdickung eines Muskelsegments zwischen Endsystole und Enddiastole. „Gerade bei einer Progression der linksventrikulären Dysfunktion bleibt die Ejektionsfraktion relativ lange stabil, während es schon frühzeitige Veränderungen gibt, die man quantifizieren kann“, erklärte Professor Dr. Sebastian Kelle, Deutsches Herzzentrum Berlin. Dazu zählt die Abnahme der longitudinalen Deformation.
Zahlreiche Studien belegen die prognostische Bedeutung der Strainanalyse. Wird der Wert bei HFpEF**-Patienten ergänzend zu Klinik und Standard-Bildgebung erfasst, kann man diejenigen mit einem erhöhten Mortalitätsrisiko besser herausfiltern.
Das Problem mit der EF
Herzschwäche bereits in frühen Stadien ausmachen
Ebenso macht er im Rahmen von Myokarditiden, nach Herztransplantationen oder in der Kardioonkologie einen Unterschied, zum Beispiel, wenn es um die kardiotoxischen Nebenwirkungen einer Chemotherapie geht. Mithilfe des Strains kann man auch asymptomatische, frühe Stadien einer Herzschwäche detektieren. Insbesondere bei Personen mit Risikofaktoren wie Diabetes oder Bluthochdruck öffnet sich dadurch ein zusätzliches diagnostisches – und therapeutisches – Fenster. Am relevantesten ist momentan der globale longitudinale Strain (GLS) als Marker der linksventrikulären Funktion. Die zirkumferentielle und radiale Deformation sollte man jedoch nicht vernachlässigen, erinnerte Professor Dr. Andreas Hagendorff vom Universitätsklinikum Leipzig. Aufgrund der unterschiedlichen Lage der Muskelfasern (longitudinal = subendomyokardial, zirkumferentiell = subepimyokardial) bietet die Analyse u.a. in der echokardiographischen Myokarditisdiagnostik einen Mehrwert, so der Ultraschall-Experte weiter.Strain via Echokardiographie ermitteln
Analog zum linksventrikulären gibt es den rechtsventrikulären Strain, mit dem man z.B. eine arrhythmogene RV-Kardiomyopathie erkennen kann. Der atriale Strain seinerseits hilft in der Differenzierung zwischen hypertropher Kardiomyopathie und Amyloidosen. Außerdem gilt eine Reduktion bei Infarktpatienten als unabhängiger Prädiktor für ein schlechteres Outcome. Die Vorhof-Kenngröße ist also mehr als nur ein Spiegelbild der Ventrikelfunktion, betonte Professor Dr. Andreas Schuster vom Herzzentrum Göttingen. Der Strain lässt sich mittels Echo, MRT oder CT ermitteln. Die Echokardiographie besticht durch eine exzellente zeitliche Auflösung – besonders wichtig für Strain-rate-Analysen. Diese Rate entspricht der Geschwindigkeit der Muskeldeformierung und dient beispielsweise der Fibrosedetektion. Zwei Optionen stehen zur Strain-Berechnung zur Verfügung: der Gewebedoppler und das 2D-Speckle (bzw. 3D-Voxel) Tracking. „Wenn man diese Verfahren standardisiert und richtig anwendet, zeigen sie eine gute Übereinstimmung“, urteilte Prof. Hagendorff. Beim Speckle Tracking werden Punkte (Speckles) während des Herzzyklus verfolgt. Das Ergebnis hängt im Gegensatz zum Doppler nicht vom Winkel ab, mit dem man schallt. Als Wermutstropfen benötigt das Verfahren eine bessere Bildqualität und eine höhere Bildrate. Betrachtet man die typische Bull’s-eye-Darstellung, weist bereits die Form der Kinetikstörung auf die Pathologie hin. Mitunter finden sich charakteristische diagnostische Muster wie das apical sparing bei einer Amyloidose. Der klinische Stellenwert des Strains steht für Prof. Hagendorff außer Frage. „Das gehört in modernen Echokardiographielaboren eigentlich zum Standard.“ Konkret empfahl der Kollege, zur Beurteilung von linkem Ventrikel und von Klappenerkrankungen mindestens den linksventrikulären Strain, in vielen Fällen auch den linksatrialen, auf dem Befund anzugeben. Bei onkologischen und KHK-Patienten kommt der rechtsventrikuläre Strain hinzu, obwohl dieser „sicherlich noch nicht zur klinischen Routine zählt“.Strain mittels MRT und CT feststellen
Die Magnetresonanztomographie umgeht das Problem schlechter Schallbedingungen. Darüber hinaus können z.B. T1- und T2-Mapping additive Informationen liefern. Den Strain erhält man auf drei verschiedenen Wegen: akquisitionsbasiert über Tagging, durch fast Strain-Encoded Imaging (fSENC) und – analog zum Speckle Tracking – via Feature Tracking. Die entsprechende Software berechnet die aus der Echokardiographie bekannten regionalen und globalen Parameter. Prof. Kelle nutzt die MR-Strainanalyse vor allem zu Follow-up-Untersuchungen. Ihm zufolge würden insbesondere jüngere oder mit einer anderen bildgebenden Modalität kaum erfahrene Kollegen von den verlässlichen Resultaten profitieren. Grundsätzlich bietet auch die Computertomographie die Möglichkeit, den Strain zu bestimmen. Und zwar nicht erst seit gestern, wie Privatdozent Dr. Mohamed Marwan vom Universitätsklinikum Erlangen ausführte. Erste Daten stammen aus dem Jahr 2010 von Patienten mit KHK. Im täglichen Betrieb spielt die Untersuchung allerdings kaum eine Rolle. Eine CT durchzuführen, nur um die LV-Funktion zu beurteilen, ist laut Dr. Marwan „nicht Sinn der Sache“. Die zeitliche Auflösung und die Notwendigkeit der Bildrekonstruktion, um funktionelle Datensätze zu generieren, limitieren den Einsatz. Nichtsdestotrotz gewinnt die CT in der Kardiologie an Bedeutung. Etabliert hat sie sich z.B. in der Planung einer Transkatheter-Aortenklappenimplantation (TAVI). Die Strainanalyse bietet sich hier aus zwei Gründen an: Einerseits liegen bei TAVI-Patienten durch die präinterventionelle Diagnostik bereits funktionelle Datensätze vor, anderseits gestaltet sich die echokardiographische Bildakquise in dieser Population schwierig. In einer Studie erhielt man den GLS via Ultraschall nur bei 54 % der Teilnehmer. Um das Outcome nach der Implantation abschätzen zu können, hat der präinterventionelle Befund aber durchaus Bedeutung.Harmonisierung der Untersuchungstechniken und Therapiepotenziale
Aus den verschiedenen Modalitäten ergibt sich für die breite klinische Anwendung des myokardialen Strains ein Problem: Zwar lassen sich die Ergebnisse gut reproduzieren, jedoch nur, wenn man bei einem Verfahren und einer Software bleibt. „Das ist einer der Schwachpunkte“, sagte Prof. Kelle. So weichen beispielsweise die Werte für den globalen zirkumferentiellen Strain innerhalb der drei MR-Messmethoden um 2,1–6,9 % voneinander ab. Diskrepanzen gibt es u.a. auch zwischen MRT und Echo. Allein die Normwerte für den linksventrikulären GLS reichen von ca. -12 % bis -22 %, weshalb man bei Verlaufskontrollen immer mit dem gleichen Gerät arbeiten sollte, betonte der Kollege. Als einen der wichtigsten Schritte der nächsten Jahre bezeichnete Prof. Schuster die Harmonisierung der Untersuchungstechniken, sodass Echo und MRT zum gleichen Resultat führen. Zudem müsse man den Strain künftig nicht nur nutzen, um Risiken zu beschreiben, sondern Therapien darauf abstimmen. Dann wird sich zeigen, ob sich die Prognose der Patienten nachhaltig verbessert.** European Society of Cardiology
*** Herzinsuffizienz mit erhaltener Ejektionsfraktion
Kongressbericht: 87. Jahrestagung der DGK (Online-Veranstaltung)