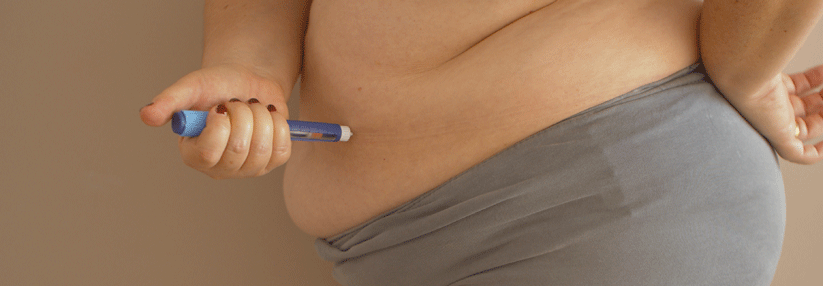
Käse statt Marmelade: Mit Gestationsdiabetes beim Frühstück Kohlenhydrate reduzieren
 Wegen der erhöhten morgendlichen Insulinresistenz sollte die werdende Mutter zum Frühstück weniger Kohlenhydrate verzehren als beim Mittag- bzw. Abendessen.
© iStock/gerenme
Wegen der erhöhten morgendlichen Insulinresistenz sollte die werdende Mutter zum Frühstück weniger Kohlenhydrate verzehren als beim Mittag- bzw. Abendessen.
© iStock/gerenme
Schwangere mit erhöhtem Stoffwechselrisiko (s. Kasten) sollten bereits vor der 24. Woche auf eine Glukosetoleranzstörung bzw. einen bisher unbekannten Diabetes gescreent werden. Ansonsten erfolgt die vorgesehene Testung in der 24.–28.Woche. Typische Symptome (Polydypsie, Polyurie, Glukosurie) erfordern zu jedem Zeitpunkt eine umgehende Abklärung, schreiben Dr. oec. troph. Heike Raab, St. Vinzenz Krankenhaus Hanau und Dr. Eckhard Klör, Diabetologische Schwerpunktpraxis, Frankfurt.
Risikofaktoren für Schwangerschaftsdiabetes
- Gestationsdiabetes in der Anamnese
- Prädiabetes bzw. Adipositas (BMI ≥ 30 kg/m2 präkonzeptionell)
- ältere Schwangere (> 35 Jahre)
- Blutdruck > 140/90 mmHg
- Polyzystisches Ovarsyndrom
- Kind mit Makrosomie (> 4500 g)
- Totgeburt in der Vorgeschichte
- mehr als drei Fehlgeburten hintereinander (habitueller Abort)
- KHK oder PAVK in der Anamnese
Ernährung mit 40–50 % Kohlenhydraten empfohlen
Bei der Diagnostik scheiden sich die Geister: Die Mutterschaftsrichtlinien sehen zunächst einen Suchtest mit 50 g Glukose vor, der auch von den Kassen bezahlt wird. Bei Werten ≥ 200 mg/dl steht die Diagnose Gestationsdiabetes (GDM) fest, bei Werten ≥ 135mg/dl ist ein 75-g-oGTT angezeigt. Die aktuelle S3-Leitlinie empfiehlt dagegen gleich einen 75-g-oGTT. Als Grenzwerte gelten ≥ 92 mg/dl (nüchtern), ≥ 180 mg/dl (nach einer Stunde) und ≥ 153 mg/dl nach zwei Stunden. Ein GDM liegt vor, wenn mindestens einer der drei Grenzwerte überschritten wird. Nach bariatrischen Operationen (z.B. Magenbypass) ist ein oGTT wegen des Dumping-Phänomens nicht möglich, ersatzweise kontrolliert man zwei Wochen lang den Blutzucker nüchtern und jeweils eine Stunde postprandial. Therapeutisch steht die Ernährungsumstellung an erster Stelle. Empfohlen wird eine Diät mit 40–50 % Kohlenhydraten, 20 % Protein (ca. 60–80 g/Tag) und 30–35 % Fett (Ernährungsberatung). Dabei verzichtet die Schwangere optimalerweise auf schnell resorbierbare Kohlenhydrate und verteilt die anderen auf drei Hauptmahlzeiten und zwei bis drei Zwischenmahlzeiten (einschließlich Spätmahlzeit), um postprandiale BZ-Spitzen zu vermeiden. Wegen der erhöhten morgendlichen Insulinresistenz empfehlen die Autoren, dass die werdende Mutter zum Frühstück weniger Kohlenhydrate verzehrt als beim Mittag- bzw. Abendessen. Außerdem sollte sie auf den glykämischen Index achten und täglichmindestens 30 g Ballaststoffe zu sich nehmen.In den ersten Wochen 1–2 kg abnehmen ist unbedenklich
Ein moderate Energiereduktion kann bei adipösen Schwangeren sinnvoll sein. Zur Prophylaxe einer ketogenen Stoffwechsellage müssen sie aber mindestens 1600–1800 kcal/ Tag aufnehmen. Eine Gewichtsabnahme von 1–2 kg in den ersten Wochen gilt als unbedenklich. Die „erlaubte“ Gewichtszunahme richtet sich nach dem BMI (s. Tabelle), bei Adipositas darf sie etwas geringer ausfallen. Zur Orientierung wiegen sich Schwangere mit GDM am besten jede Woche und schreiben ihr Gewicht auf.| Erlaubte Gewichtszunahme | |
|---|---|
| BMI (kg/m2) | Gewichtszunahme |
| < 18,5 | 12,5–18 kg |
| 18,5–24,9 | 11,5–16 kg |
| 25–29,9 | 7–11,5 kg |
| ≥ 30 | 5–9 kg |
Unerlässlich: die regelmäßige Blutzucker- Selbstkontrolle. Die Zielwerte liegen nüchtern und präprandial zwischen 65 und 95 mg/dl, eine Stunde postprandial ≤ 140 mg/dl und zwei Stunden danach bei ≤ 120 mg/dl. Der HbA1c-Wert eignet sich nicht zur Überwachung eines Schwangerschaftsdiabetes.
Fest zum Therapiekonzept gehört auch eine moderate sportliche Aktivität – außer bei Kontraindikationen wie Präeklampsie und Schwangerschaftshochdruck. Am leichtesten lässt sich zügiges Spazierengehen umsetzen (mindestens dreimal in der Woche 30 Minuten). Kurze Bewegungseinheiten (20–30 Minuten) nach denHauptmahlzeiten bremsen den postprandialen BZ-Anstieg.
Insulin benötigen etwa 20–30 % der Schwangeren mit GDM. Die hormonelle Therapie ist indiziert, wenn die Zielwerte trotz Ernährungsumstellung und Bewegung verfehlt werden. Nicht zuletzt wegen der geburtsmedizinischen Konsequenzen (nötige Geburtseinleitung am Termin etc.) raten die Autoren allerdings, die Indikation streng zu stellen (Diät-Compliance prüfen). Eine Therapie mit Basalinsulin wird empfohlen, wenn der Nüchternblutzucker wiederholt 110 mg/ dl übersteigt oder 50 % der Werte innerhalb einer Woche zu hoch sind. Ein kurz wirksames Insulin brauchen die Frauen, wenn die Hälfte der postprandialen Glukosespiegel die Norm überschreitet. Schwangeren mit Insulintherapie raten die Autoren dringend, in einer Klinik mit Neonatologie zu entbinden.
Auch bei normalem Blutzucker nach Geburt noch mal testen
Große Bedeutung hat die kontinuierliche Nachsorge, denn 35–60 % der Betroffenen entwickeln in den folgenden zehn Jahren einen Typ- 2-Diabetes. Da sich die Glukosetoleranzstörung oft nicht vollständig zurückbildet, wird auch bei normalen BZ-Werten 6–12 Wochen nach der Geburt ein 75-g-oGTT empfohlen. Außerdem ist eine jährliche Bestimmung von Nüchtern-BZ und HbA1c vorgesehen sowie ein oGTT alle zwei Jahre und vor einer erneuten Schwangerschaft. Als ausgesprochen günstig hat sich bei Mütternmit GDMdas Stillen erwiesen, es verringert das Risiko für einmetabolisches Syndrom noch bis zu 15 Jahre nach der Entbindung.Quelle: Raab H, Klör E. Ernährungs Umschau 2020, 2: M110-118; DOI: 10.4455/eu.2020.013














