Lysosomale Speicherkrankheiten richtig erkennen und behandeln
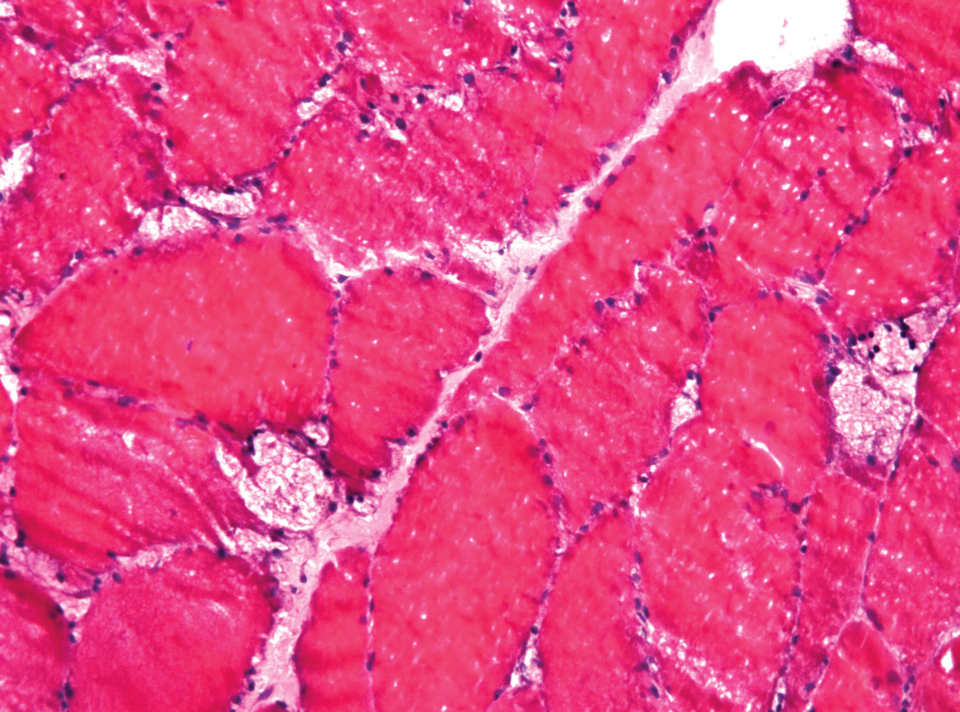
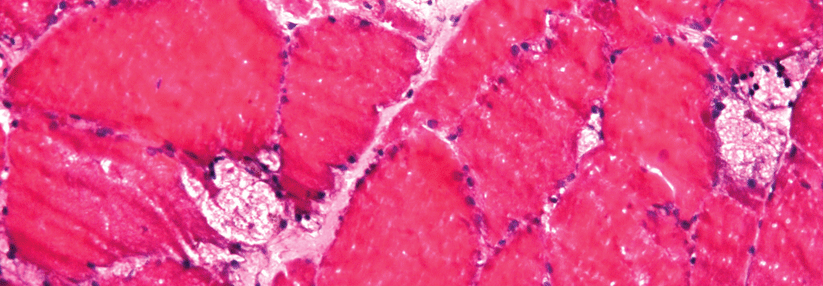 Beim Morbus Pompe werden die Speichervakuolen in den Muskeln riesig. Dadurch können sie nicht mehr richtig arbeiten.
© wikimedia/Jensflorian
Beim Morbus Pompe werden die Speichervakuolen in den Muskeln riesig. Dadurch können sie nicht mehr richtig arbeiten.
© wikimedia/Jensflorian
Bei lysosomalen Speicherkrankheiten kommt es zur Akkumulation von Glykosaminoglykanen, Glykoproteinen oder Glykolipiden in diversen Geweben des Körpers. Die Folge ist eine progressive Organschädigung. Die Vererbung erfolgt meist autosomal-rezessiv. Lysosomale Speicherkrankheiten können auch nur leicht ausgeprägt sein und/oder erst im Erwachsenenalter auftreten bzw. diagnostiziert werden.
Morbus Gaucher
Patienten mit Morbus Gaucher Typ 3 mangelt es an dem Enzym b-Glucosidase, wodurch es zu einer Akkumulation von Glykolipiden in den Lysosomen kommt. Die Infiltration lipidbeladener Makrophagen (Gaucher-Zellen) führt zu einer interstitiellen Lungenerkrankung. Außerdem kann sich infolge der Okklusion von Kapillaren eine pulmonale Hypertonie entwickeln. Zusätzlich verringern Hepatomegalie und Wirbelsäulenverkrümmung das Lungenvolumen, schreibt das Team um Dr. Aleksandra Jezela-Stanek vom Nationalen Institut für Tuberkulose und Lungenerkrankungen in Warschau.
Die Enzymersatztherapie (ERT) führte in Fallberichten und Studien zu widersprüchlichen Ergebnissen. In einer kleinen Fallserie verringerte sie weder Inzidenz noch Progression der interstitiellen Lungenerkrankung. Auch bei einem elf Jahre lang mit ERT behandelten Patienten zeigte sich eine pulmonale Progression, aber Leber- und Milzwerte waren fast normal. Möglicherweise hilft eine Transplantation: Bei einem Patienten wurden auch sechs Jahre nach der Transplantation keine Gaucher-Zellen im Spenderorgan nachgewiesen.
Niemann-Pick-Krankheit
Eine weitere Lipidspeicherkrankheit mit pulmonalen Komplikationen ist der Morbus Niemann-Pick Typ B – ausgelöst durch eine verringerte Aktivität der sauren Sphingomyelinase. Drei von vier Patienten leiden an einer interstitiellen Lungenkrankheit. Zur Wirkung der Enzymersatztherapie gibt es bisher nur wenige Daten. Zwei kleinere Arbeiten ermittelten eine Verbesserung der Diffusionskapazität um rund 13 % und eine Reduktion typischer Veränderungen in der hochauflösenden Computertomographie.
Morbus Pompe
Mit pulmonalen Folgen muss man auch beim Morbus Pompe rechnen, dem ein α-Glukosidase-Mangel zugrunde liegt. Die vermehrte Glykogenspeicherung schwächt oft schon frühzeitig die Atemmuskulatur. Die Folge ist eine chronische respiratorische Insuffizienz bis hin zur Beatmungspflicht. Inzwischen gibt es ermutigende Daten zur Enzymersatztherapie: Zwei Drittel der „Late-Onset“-Patienten profitieren davon. Die Enzymersatztherapie kann Atemfunktion und Belastbarkeit verbessern und das Überleben verlängern.
Sechs Pathomechanismen
- Infiltration durch abnormale Zellen (Gaucher Typ 3, Niemann-Pick-Krankheit)
- muskuläre Schwäche (Morbus Pompe)
- verringerte Thoraxbeweglichkeit durch Versteifung von Haut und Ligamenten (Mukopolysaccharidosen)
- Verdrängung der Lunge durch Hepatomegalie (Gaucher Typ 3, M. Niemann-Pick, Mukopolysaccharidosen)
- Wirbelsäulen-Deformitäten (Gaucher Typ 3, Mukopolysaccharidosen)
- rezidivierende Atemwegsinfekte
Mukopolysaccharidosen
Zu den lysosomalen Speicherkrankheiten mit Lungenbeteiligung zählen auch die Mukopolysaccharidosen. Bei diesen mangelt es an Enzymen zum Abbau von Glykosaminoglykanen. Eine Beteiligung des Respirationstrakts zeigen alle Patienten. Die Ursachen reichen von verdickter Zunge und flacher Nasenwurzel bis zu neurologischen Defiziten. Dadurch kann es zu einer progredienten respiratorischen Insuffizienz sowie zu einer schweren Schlafapnoe und zentralen Apnoe kommen. Eine Enzymersatztherapie verringert unabhängig vom Mukopolysaccharidose-Typ die Zahl der Atemwegsinfekte. Möglicherweise kann sie bei ausgewählten Patienten auch die Lungenfunktion bessern und die Progression aufhalten.Morbus Fabry
Bei Patienten mit Morbus Fabry wird die lysosomale Lipidspeicherung durch einen α-Galaktosidase-Mangel ausgelöst. Ersten Daten zufolge entwickelt knapp die Hälfte der Betroffenen eine bronchiale Obstruktion, wobei sich die Lungenfunktion meist nur langsam verringert. Männer sind von der X-chromosomal vererbten Krankheit stärker betroffen als Frauen. Die Enzymersatztherapie sollte möglichst früh begonnen werden. Allerdings scheint der Effekt auf die pulmonale Beteiligung begrenzt zu sein. Das liegt möglicherweise daran, dass die Lungenschäden bei Morbus Fabry überwiegend entzündlich bedingt sind.Quelle: Jezela-Stanek A et al. Clin Respir J 2020; DOI: 10.1111/crj.13150