Big-Data-Projekt erhöht Evidenzlage zur AML
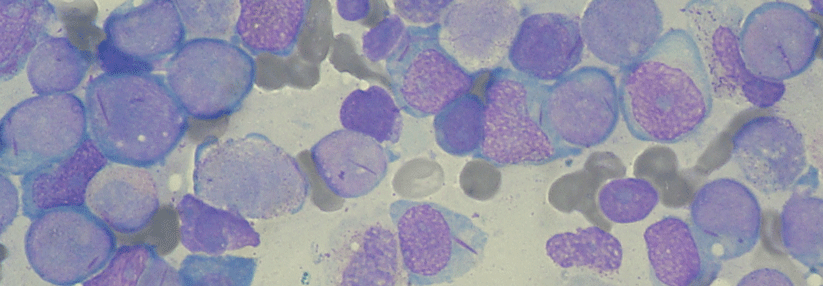
 In HARMONY wurden die Daten von 3000 AML-Patienten beleuchtet und miteinander verglichen.
© iStock/alphaspirit
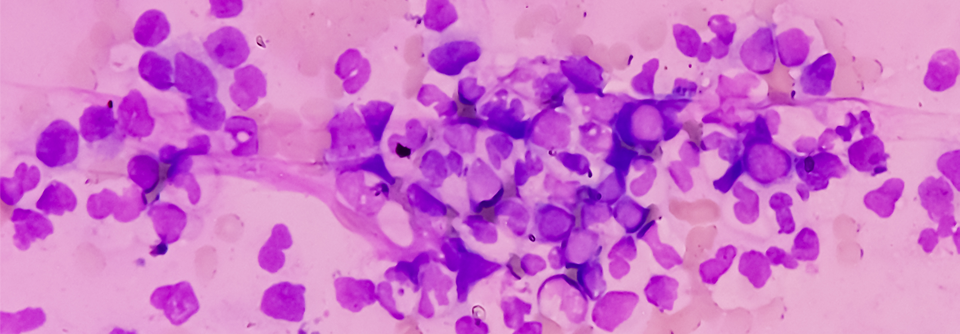
In HARMONY wurden die Daten von 3000 AML-Patienten beleuchtet und miteinander verglichen.
© iStock/alphaspirit
Um die Entwicklung neuer Behandlungsoptionen und die personalisierte Betreuung zu beschleunigen, werden in einer großen Datenbank Informationen über sehr viele Patienten gesammelt und ausgewertet. Das dazugehörige Pilotprojekt zur akuten myeloischen Leukämie (AML) stellte Professor Dr. Lars Bullinger, Medizinische Klinik m.S. Hämatologie, Onkologie und Tumorimmunologie, Charité – Universitätsmedizin Berlin, vor.
Es umfasst unter anderem, wie Gen-Gen-Interaktionen die Prognose der Erkrankten verändern. So spielt der Mutationsstatus zahlreicher Gene bei der AML eine wichtige Rolle. Doch in den letzten Jahren sei klar geworden, so Prof. Bullinger, dass sich Mutationen in verschiedenen Genen gegenseitig stark beeinflussen. Zum Beispiel kann eine FLT3-ITD-Mutation die günstige prognostische Rolle einer NPM1-Mutation konterkarieren.
Aufgrund der COVID-19-Restriktionen flossen in die ersten Resultate Mitte Juni statt der geplanten etwa 5000 nur knapp 3000 Patienten ein, bedauerte der Referent. Jedoch würde dies bereits die Zahlen der bislang größten klinischen AML-Studien übertreffen, betonte Prof. Bullinger.
Das steckt hinter HARMONY
Weitere Unterteilung bereits bekannter Risikogruppen
Die Analysen zeigten neben dem bekannten Muster gemeinsam auftretender bzw. sich gegenseitig ausschließender Mutationen auch interessante neue Befunde: So kam die Koexistenz von Mutationen in den Genen EZH2 und RUNX1 oder von RUNX1-Mutationen mit aberranten Splicing-Vorgängen z.B. in SRSF2, SF3B1 und STAG2 zutage. Dem Berliner Arzt zufolge gestatten die Daten außerdem die noch feinere Aufspaltung scheinbar bereits gut charakterisierter Risikogruppen:- So wurden 268 AML-Patienten mit einer Inversion auf Chromosom 16 gefunden, die größtenteils die bekannte gute Prognose aufweisen. Allerdings lassen sich zwei kleinere Untergruppen anhand bestimmter zusätzlicher Mutationskombinationen abspalten, die hinsichtlich des Überlebens deutlich schlechter abschneiden.
- Erkrankte mit PTPN11-, aber ohne NPM1-Mutation haben gewöhnlich eine schlechte und solche mit NPM1-, aber ohne PTPN11-Mutation eine intermediäre bis gute Prognose. Liegen beide Aberrationen vor, so sind die Aussichten noch besser als mit alleiniger NPM1-Mutation.
- Erhalten Patienten mit PTPN11-Mutation und NPM1-Wildtyp eine allogene Stammzelltransplantation, verdoppelt sich trotz prognostisch ungünstigster Konstellation die mediane Überlebensdauer. Patienten mit NPM1- und DNMT3A-Mutationen profitieren hingegen nur von dem Eingriff, wenn gleichzeitig eine Mutation im Gen RAD21 vorliegt.
Bestimmt der MRD-Status die Prognose langfristig?
Ein weiteres neues HARMONY-Projekt zur AML beinhaltet die Rolle der minimalen Resterkrankung (MRD), sagte der Hämatologe Professor Dr. Gert Ossenkoppele, Amsterdam University Medical Centers. Der Nachweis einer MRD nach Therapieende gilt als ungünstiger Prognosefaktor. Nun wird auf Basis eines großen Kollektivs aus zahlreichen europäischen Studiengruppen eine Metaanalyse durchgeführt, um ein für alle Mal zu klären, ob sich der MRD-Status in klinischen Studien als Surrogatmarker für das Gesamtüberleben bei AML einsetzen lässt. Der Vorteil liegt auf der Hand: Eine mögliche MRD-Negativität ist bereits kurz nach Ende der Therapiephase nachweisbar, während bis zum Auftreten eines Überlebensvorteils oft Jahre vergehen. Sollte ein Zusammenhang zwischen MRD-Negativität und langfristiger Prognose daher zweifelsfrei bestehen, könnte das die Entwicklung und Zulassung neuer Therapien enorm beschleunigen, so Prof. Ossenkoppele.Quelle: Bullinger L, Ossenkoppele G. Virtuelles EHA-Webinar „The Power of Integrating Harmonized AML Patient Data in Hematology Research”