Gliomklassifikation mittels Liquid Biopsy Hirntumor: Hin zu einer nichtinvasiven Diagnostik
 Die Liquid Biopsy mit Methylierungsanalysen könnte zukünftig bei Gliom-Diagnosen helfen.
© Tryfonov – stock.adobe.com
Die Liquid Biopsy mit Methylierungsanalysen könnte zukünftig bei Gliom-Diagnosen helfen.
© Tryfonov – stock.adobe.com
Gliome früh zu erkennen, ist schwierig, Biopsien sind risikobehaftet, die Histopathologie manchmal ungenau. So begründete Dr. Dr. Yan Sun von der Universität Maastricht den klinischen Bedarf für eine nichtinvasive diagnostische Methode.1 Gleichzeitig erschwert die Blut-Hirn-Schranke den Nachweis von zirkulierender Tumor-DNA.
Mit dem Ziel, dennoch eine „sichere und akkurate“ Aussage per Liquid Biopsy zu ermöglichen, analysierte das Team um Dr. Sun zunächst umfassend die DNA-Methylierungsmuster von Gliomen, Nicht-ZNS-Tumoren und gesunden Geweben.
Was wurde untersucht?
Anhand eines Datensatzes, der insgesamt mehr als 15.000 Proben umfasste, prüfte das Team, welche Performance verschiedene Algorithmen aus dem Bereich des maschinellen Lernens und Deep Learning bei der Gliomklassifikation erbringen. Die Forschenden erarbeiteten zudem einen Basisdatensatz zu typischen Methylierungs-Sites und möglichen neuen Biomarkern.
Die besten Ergebnisse bei der Gliom-Subtypklassifikation lieferte ein „Transformer“-basiertes Modell. Für häufige Tumortypen lag dessen Genauigkeit bei 98,06 %, berichtete Dr. Sun. Allerdings war das Modell bisher rein mit Gewebeproben trainiert worden. „Die Frage ist: Können wir die Methodik vom Gewebe auf den Nachweis aus Blutplasma übertragen?“ Ein Abgleich der differenziell methylierten Loci in zellfreier DNA aus Blutproben von Gliompatient:innen habe ergeben, dass sich die wichtigsten Methylierungs-Biomarker auch im Blut nachweisen lassen. Darunter spezifische Marker für das Grading und molekulare Gliomsubtypen. An der Validierung und Entwicklung eines Diagnostiktools werde aktuell gearbeitet.
Wann kann ein Methylierungsprofiling helfen?
Die Arbeit mache deutlich, was mit Data-Mining-Bemühungen alles möglich sei, kommentierte Prof. Dr. Michael Weller vom Universitätsspital Zürich.2 Zwei Grundsatzfragen seien nun:
- Wie ausgereift ist die Anwendung des DNA-Methylierungsprofiling in der Tumordiagnostik und inwieweit wird es von der klinischen Gemeinschaft angenommen?
- In welchen Situationen wäre man bereit, mit den Informationen aus Liquid Biopsies zu arbeiten und sie für klinische Entscheidungen heranzuziehen?
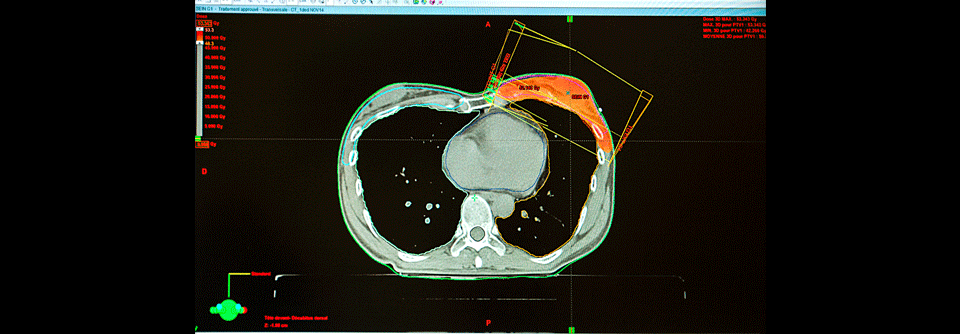
Als mögliches Anwendungsgebiet nannte der Diskutant unklare Bildgebungsbefunde, z. B. nach Hochdosis-Strahlentherapien. „Wenn wir den Erkrankten erklären: ‚Wir wissen nicht, ob es eine Pseudoprogression oder eine echte ist, wir machen in acht Wochen wieder einen Scan‘, dann ist das wissenschaftlich solide – für die Betroffenen allerdings nicht ideal.“ Ein Blutbiomarker könne da durchaus nützlich sein.
Quellen:
1. Sun Y et al. ESMO Congress 2025; Abstract 665MO
2. Weller M. ESMO Congress 2025; Invited Discussant 665MO and 666M