PML: Diagnose und Therapie
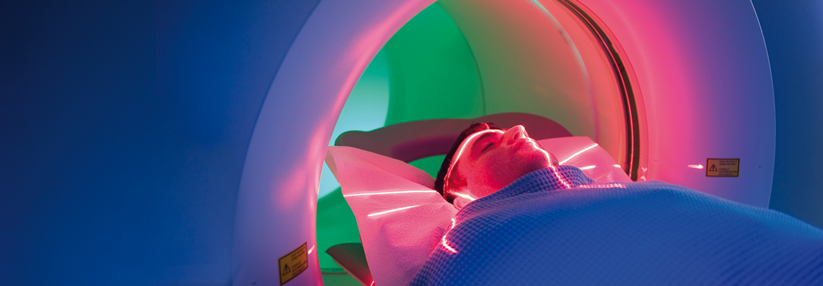 MS-Patienten unter Natalizumab müssen regelmäßig ins MRT, damit PML-Läsionen nicht erst in diesem späten Stadium erkannt werden.
© iStock.com/baranozdemir
MS-Patienten unter Natalizumab müssen regelmäßig ins MRT, damit PML-Läsionen nicht erst in diesem späten Stadium erkannt werden.
© iStock.com/baranozdemir
Die progressive multifokale Leukencephalopathie (PML) ist eine demyelinisierende Infektion des zentralen Nervensystems, die durch Reaktivierung des JC-Virus ausgelöst wird. Betroffen sind Patienten mit einer gestörten zellulären Immunabwehr – z.B. im Rahmen von AIDS, verschiedenen Krebserkrankungen, nach Stammzell- und Organtransplantation oder durch bestimmte immunsuppressiv wirkende Medikamente wie Natalizumab.
Trotz negativer PCR werden Patienten symptomatisch
Die Erkrankung führt zu fortschreitenden kognitiven Einschränkungen, motorischen Defiziten, Ataxie und Sehstörungen und endet praktisch immer tödlich, wenn es nicht gelingt, die zelluläre Immunfunktion wiederherzustellen.1
Wird die PML früh erkannt, ist mit besseren Überlebenschancen und einem besseren neurologischen Outcome der Betroffenen zu rechnen. Für MS-Patienten unter Natalizumab sind daher regelmäßige MRT-Kontrollen vorgesehen. Das Ziel: Kleine PML-Läsionen erkennen, die noch nicht zu Symptomen geführt haben. Inwieweit die Größe dieser Läsionen mit einem positiven PCR-Nachweis von JCV-DNA im Liquor cerebrospinalis assoziiert ist, untersuchten Neurologen um Dr. Martijn Wijburg, Vrije Universiteit Amsterdam.2
An der retrospektiven Studie nahmen insgesamt 56 mit Natalizumab behandelte MS-Kranke teil, bei denen die Diagnose PML gestellt worden war. Als Kriterien dafür galten ein positiver JCV-Nachweis plus verdächtige MRT-Befunde. War die Virus-PCR negativ, mussten folgende vier Kriterien erfüllt sein:
- hohes PML-Risiko, d.h. positiver Anti-JCV-Serostatus und Natalizumabtherapie > 12 Monate
- keine MS-Aktivität vor dem PML-Verdacht
- im MRT PML-typische Hirnläsionen bei Abwesenheit von Befunden, die für andere Erkrankungen charakteristisch sind
- PML-Verdacht auch im Kontroll-MRT
Wie die niederländischen Kollegen berichten, entwickelten 37 der 47 Patienten mit positiver JCV-PCR in der Nachbeobachtungszeit von mindestens sechs Monaten klinische Symptome. Bei neun Kranken war die PCR initial negativ, dennoch wurden fünf von ihnen im Verlauf symptomatisch.
Hoffnungsschimmer am Therapiehorizont
Was den Zusammenhang zwischen dem PML-Läsionsvolumen und dem Ergebnis der PCR anging, fanden die Wissenschaftler Folgendes heraus:
- MS-Patienten mit positiver PCR hatten ein größeres Gesamt-Läsionsvolumen als diejenigen mit negativer PCR (22,9 ml vs. 6,7 ml).
- Bei geringem Läsionsvolumen war die Wahrscheinlichkeit, dass die PCR negativ ist, deutlich höher.
- Zwischen Läsionsvolumen und Zahl der JCV-Kopien bestand eine positive Korrelation.
- Symptomatische Patienten wiesen ein größeres Läsionsvolumen und eine stärkere Disseminierung der Läsionen auf.
- Ein Zusammenhang zwischen positiver PCR und Symptomen war nicht zu erkennen.
Diese Erkenntnisse erleichtern nicht gerade die PML-Diagnose im Rahmen der Pharmakovigilanz, räumen die Autoren ein. Bei kleinem Läsionsvolumen sei die PCR häufiger negativ und die PML öfters asymptomatisch, was die Erkrankung aber keinesfalls ausschließe. Dies könne zu diagnostischen und therapeutischen Unsicherheiten führen. In solchen Fällen sei man dann auf die sorgfältige klinische Beobachtung des Patienten plus wiederholter MRT- und PCR-Kontrollen angewiesen. Dr. Wijburg et al. hoffen daher auf zusätzliche diagnostische Möglichkeiten wie die Bestimmung von JVC-Antikörpern im Liquor oder einen sensitiveren PCR-Assay.
Hoffnung haben auch Dr. Muharrem Muftuoglu und seine Kollegen vom M.D. Anderson Cancer Center in Houston – Hoffnung, dass sich ihre ersten positiven Therapieergebnisse bei JCV-Infektion in weiteren Studien bestätigen werden.1 Die Wissenschaftler behandelten drei PML-Patienten mit spezifischen T-Zellen gegen das BK-Virus.
Dieses Virus gehört wie JCV zu den Polyomaviren und weist eine große genetische Ähnlichkeit auf. BK-Viren führen bei Patienten nach Stammzell- und Organtransplantationen zu Zystitis und Nephritis. BK-virusspezifische T-Zellen wurden von verschiedenen Arbeitsgruppen bereits erfolgreich dagegen eingesetzt. Nun also die ersten Versuche mit diesen kryokonservierten, teilweise HLA-gematchten T-Zellen bei der PML. Behandelt wurden:
- eine 32-Jährige mit akuter myeloischer Leukämie (AML), bei der man 20 Monate nach einer Nabelschnurblut-Transplantation die PML festgestellt hatte
- eine 73-Jährige, die aufgrund einer Polycythaemia rubra vera seit über acht Jahren auf den JAK-1/2-Inhibitor Ruxolitinib eingestellt war
- ein 35-Jähriger mit AIDS
BK-virusspezifische T-Zellen als Waffe gegen die PML?
Bei allen drei Patienten kam es schon nach der ersten Infusion zu einem deutlichen Rückgang der JC-Virus-Last im Liquor. Bei der AML-Patientin war nach zwei weiteren Infusionen gar kein Virus mehr nachweisbar und die klinischen Symptome und Befunde in der Bildgebung bildeten sich zurück. 24 Monate nach der letzten Infusion war sie weiterhin asymptomatisch.
Auch bei der alten Dame ging die Viruslast nach der zweiten Infusion weiter zurück – es zeigte sich aber keine Verbesserung des klinischen Befundes und der Bildgebung. Sie verstarb nach acht Monaten. Der junge AIDS-Patient erhielt drei weitere Infusionen, die zu einer vollständigen Virus-Clearance im Liquor führten. Auch bei ihm besserten sich die Symptome deutlich. Nach neun Monaten lief der Mann, der vorher noch nicht mal ohne Hilfe sitzen konnte, eigenständig am Stock. Möglicherweise hat man mit den BK-virusspezifischen T-Zellen eine Waffe gegen die PML gefunden, spekulieren Dr. Muftuoglu und seine Kollegen. Die ermutigenden Ergebnisse sollen jetzt in weiteren Studien überprüft werden.
Quelle:
1. Muftuoglu M et al. N Engl J Med 2018; 379: 1443-1451
2. Wijburg M et al. JAMA Neurol 2018; 75: 827-833