Darmkrebs Erhöhte Tumorkontrolle in Phase-1/2-Studie
 Die KRASG12C-Mutation gilt als Ursache der Resistenz gegen EGFR-Inhibition.
© iStock/Dr_Microbe
Die KRASG12C-Mutation gilt als Ursache der Resistenz gegen EGFR-Inhibition.
© iStock/Dr_Microbe
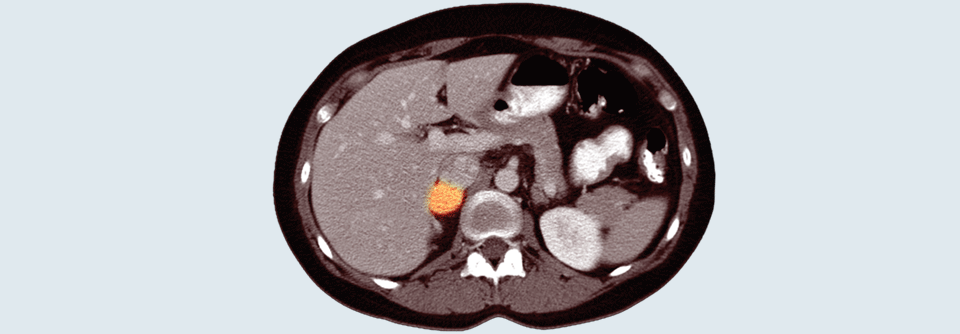
In 3–4 % aller kolorektalen Karzinome ist die KRASG12C-Mutation als onkogener Treiber nachweisbar. „Diese Mutation ist prädiktiv für eine geringe Effektivität von Cetuximab“, erläuterte Professor Dr. Jared Weiss von der University of North Carolina in Chapel Hill. Mit Adagrasib wurde ein selektiver, kovalenter Inhibitor des mutierten KRASG12C entwickelt. Er fixiert das Protein irreversibel in seinem inaktiven Zustand, hat eine lange Halbwertszeit von rund 24 Stunden, eine dosisabhängige Pharmakokinetik und durchdringt die Blut-Hirn-Schranke.
In-vivo-Forschungsdaten zufolge resultiere die Ergänzung der EGFR-Blockade durch eine gleichzeitige Inhibition der KRASG12C-Mutation im nachfolgenden…
Bitte geben Sie Ihren Benutzernamen und Ihr Passwort ein, um sich an der Website anzumelden.