Warum die CE-Markierung überdacht werden sollte
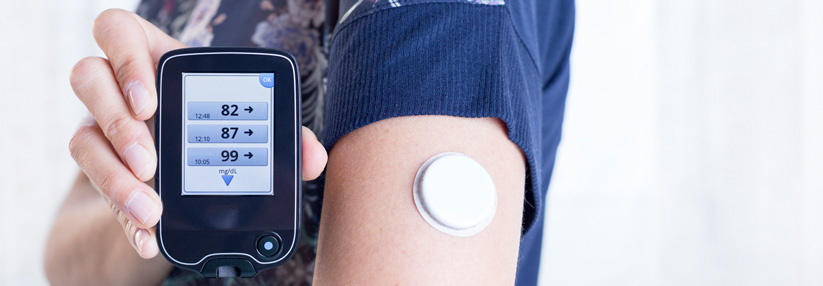
 Medizinprodukte sind nicht mit Konsumgütern gleichzusetzen. Und doch gleichen sich die Produktionsprozesse.
© Gemeinfrei (wikimedia)/MT
Medizinprodukte sind nicht mit Konsumgütern gleichzusetzen. Und doch gleichen sich die Produktionsprozesse.
© Gemeinfrei (wikimedia)/MT
Ende November beschäftigte sich Medienberichten zufolge ein internationales Journalistenkonsortium mit der Qualität von Medizinprodukten und setzte sich dabei kritisch mit Zulassungsverfahren in Deutschland und Europa auseinander – hier wurden auch Beispiele aus der Diabetologie genannt. So stellte eine Reportage anekdotisch den bedauerlichen Fall einer Hypoglykämie eines jungen Patienten dar, dessen Insulinpumpe angeblich selbstständig zehn Einheiten Insulin abgegeben haben soll und damit das Leben des jungen Patienten gefährdete.
Auch kam es in dem Beitrag zur Diffamierung eines geschätzten deutschen Diabetologen und zu Zweifeln, ob die Insulinpumpentherapie überhaupt bei jungen Patienten gerechtfertigt ist. Die DDG hat am 10.12.2018 auf Letzteres umgehend reagiert und in einer Pressemitteilung die positiven Aspekte der Behandlung von Patienten mit Typ-1-Diabetes mit Insulinpumpen aufgezeigt.
Diese Diskussion bietet einen guten Anlass, sich etwas gründlicher mit der Qualität von Diabetestechnologie und den aktuellen Zulassungsverfahren zu beschäftigen.
Benannte Stelle für Zulassung frei wählbar
Während in den USA eine mächtige und unabhängige Behörde namens FDA sämtliche Zulassungsverfahren für pharmakologische und medizintechnische Produkte regelt, reicht in Europa für technische Produkte eine Art Schmalspurzulassung aus – die sogenannte CE-Markierung. Neben Toastern oder Mixern fallen unter dieses Zulassungsverfahren auch Medizinprodukte aller Art.
Das Zulassungsverfahren scheint denkbar einfach: Notwendig sind technische Beschreibungen des jeweiligen Gerätes; eine zuständige „benannte Stelle“ kann der jeweilige Hersteller selbst aussuchen. Diese wiederum verfolgt mit ihrem Service ein Geschäftsmodell. So entsteht dort der Druck, die CE-Zertifizierung möglichst reibungslos und niedrigschwellig zu gestalten.
Klinische Studien im Vorfeld der Zulassung sind nicht in jedem Fall erforderlich, der Hinweis auf ähnliche, bereits CE-markierte Vergleichsprodukte reicht häufig aus. Natürlich lassen sich Insulinpumpen oder CGM-Systeme nicht mit Mixern oder Toastern auf eine Qualitätsstufe stellen. Während es bei Konsumgütern mehr darum geht, dass diese ohne Gefahr angewendet werden können, müssen an medizinischen Produkten zusätzliche Anforderungen gestellt werden.
Das betrifft die klinische Zuverlässigkeit, bei Messsystemen die Messgenauigkeit, bei Medikamentenabgabesystemen die Abgabegenauigkeit, auch einen qualitativ hochwertigen Herstellungsprozess und sogar den Prozess des Recyclings. Solche Prozesse sind zu fordern, denn sie müssen die Sicherheit der Patienten gewährleisten. Allerdings sollten sie schnell genug sein, um den Patienten die innovativen Produkte oder Methoden zeitnah zur Verfügung zu stellen. Es darf nicht sein, dass die Innovationen deutlich schneller vorankommen als die notwendigen Zulassungsprozesse.
Die aktuelle Situation ist also äußerst unbefriedigend, vor allem für die Patienten. Zwar hat die Europäische Union die Bedingungen für die Erlangung einer CE-Markierung verschärft, die Notwendigkeit von klinischen Studien gibt es aber nicht bei allen Produkten. Unangetastet bleiben dabei der rechtliche Status und das Geschäftsmodell der „benannten Stellen“. Eine zentrale Behörde, ähnlich der Europäischen Arzneimittelagentur für pharmazeutische Produkte, für den Medizinproduktemarkt aufzubauen, ließ sich leider politisch nicht durchsetzen: „Zu viel Bürokratie“, so hieß es – und Einzelgänge der Länder sind nicht erwünscht und auch wenig sinnvoll.
In Studien nachgewiesene Qualität per Siegel ausweisen
Unabdingbar ist es, dass in einem Neugestaltungsprozess die Fachgesellschaften die wesentliche Rolle spielen. Die EASD hat bei der Jahrestagung 2018 in Berlin eine Initiative zum Umgang mit Technologie ins Leben gerufen und führt aktuell Gespräche mit den Meinungsbildnern in verschiedenen Ländern. Vorstellbar wäre eine Art Gütesiegel für Produkte von Herstellern, die ihre Qualität in klinischen Studien nachgewiesen haben. Konsequent durchgeführt, könnte dies mittelfristig dazu führen, dass die Spitzenverbände der Krankenkassen die Kostenübernahme für Produkte mit Gütesiegel gewähren.