Krampfanfälle, Magenschmerzen, Flush – neuroendokrine Tumoren schießen mit Hormonen um sich
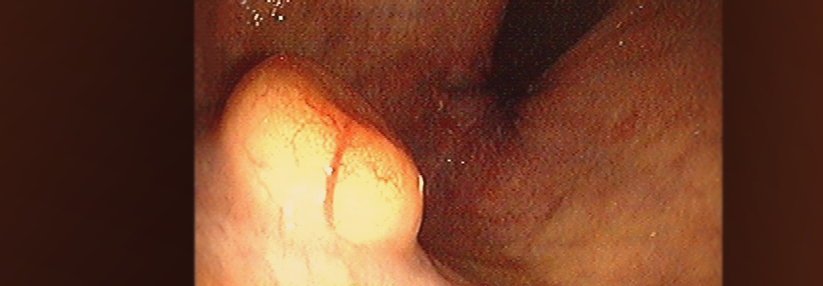 Ein Karzinoid im Rektum eines Patienten. Welche ist die richtige Therapieoption?
© Albertinen-Krankenhaus Hamburg/endoskopie-bilder.de
Ein Karzinoid im Rektum eines Patienten. Welche ist die richtige Therapieoption?
© Albertinen-Krankenhaus Hamburg/endoskopie-bilder.de
Neuroendokrine Neoplasien (NEN) finden sich am häufigsten im Gastrointestinaltrakt (60 %). Sieben von zehn Patienten entwickeln zwar kein Hormonsyndrom, bei den übrigen drei ist der Tumor aber funktionell aktiv und schüttet unkontrolliert Hormone aus.
Oft wird ein NEN zufällig entdeckt, weil der Patient z.B. zu einer Routine- oder Vorsorgekoloskopie kommt. Auch Appendektomien fördern ab und an solche Neoplasien zutage, schreiben Privatdozent Dr. Lutz P. Breitling von der Klinik für Gastroenterologie und seine Kollegen vom Universitätsklinikum Marburg. Sie stellen NEN-Lokalisationen im Rahmen der drei häufigsten Hormonsyndrome vor.
Bei Pankreas-NEN handelt es sich oft um ein Insulinom, das auch das gleichnamige Syndrom auslöst. Es ist zwar bei neun von zehn Patienten benigne, aber durch den Überschuss an Insulin kommt es zu Hypoglykämie-Symptomen. Die Beschwerden reichen von Schweißausbrüchen, Schwäche und Tremor bis zu Verwirrtheit, Krampfanfällen und Koma.
Beim Gastrinom genügen mitunter schon PPI
Ebenfalls im Pankreas oder im Duodenum entwickelt sich das Gastrin ausschüttende Gastrinom. Seine Malignität liegt bei 50–80 %. Es führt zu einem Zollinger-Ellison-Syndrom (Magensäurehypersekretion), was sich über abdominelle Schmerzen (peptischer Ulkus), Reflux und Diarrhö bemerkbar macht. Obere gastrointestinale Blutungen, Erbrechen und Gewichtsverlust können ebenfalls auf ein Gastrinom hinweisen.
Fasten und Sekretin geben
- Wer ein Insulinom befürchtet, lässt seinen Patienten testweise hungern: Während des Fastens bleiben Insulin- und C-Peptid-Spiegel trotz niedriger Glukosewerte unnormal erhöht.
- Dem Zollinger-Ellison-Syndrom kommt man über einer Sekretin-Gabe auf die Spur, wenn dadurch das Gastrin ansteigt.
Gestörtes Labor
- Die PPI-Therapie führt bei der Verlaufskontrolle mit Chromogranin A oft zu falsch hohen Werten.
- Kaffee, Tee, Schokolade, Aubergine, Avocado, Banane und Ananas lassen die Werte von 5-Hydroxyindolessigsäure (5-HIES) steigen. Bei fortgeschrittenen Dünndarmtumoren liegt die Sensitivität des Markers bei 70–75 % und die Spezifität bei 85–100 %.
Oft ist eine lebenslange Nachsorge notwendig
Eine Reduzierung der Tumorlast oder der funktionellen Symptome lässt sich mittels Embolisation erreichen, z.B. im Fall von inoperablen Lebermetastasen. Bei einigen Patienten eignen sich lokal-ablative bzw. lokoregionäre Verfahren auch zur kurativen Therapie. Zur Auswahl stehen Radiofrequenzablation, transarterielle Embolisation und Chemoembolisation.Ab in den OP
Quelle: Breitling LP et al. Dtsch Med Wochenschr 2019; 144: 1509-1521; DOI: 10.1055/a-0865-0061