Bei Immuncheckpointhemmern zählt auch Diabetes zu den Nebenwirkungen
 PD1-Antikörper zerstören u.a. den natürlichen Schutzmechanismus von Betazellen.
© ugreen – stock.adobe.com
PD1-Antikörper zerstören u.a. den natürlichen Schutzmechanismus von Betazellen.
© ugreen – stock.adobe.com
Tumorzellen exprimieren Neoantigene, die von dendritischen Zellen aufgenommen und den naiven T-Zellen im Lymphknoten präsentiert werden. T-Zellen lernen so, den Feind zu erkennen. „Amplitude und Qualität der T-Zell-Antwort werden ausbalanciert, indem Kostimulatoren das System aktivieren oder Checkpoints hemmende Signale setzen“, erklärte Privatdozentin Dr. Susanne Reger-Tan, Universitätsklinikum Essen. Diese Immunreaktion wird per Feedback über CTLA4 reguliert.
Schutz eigener Gewebe wird geschwächt
Tumorzellen selbst erzeugen ein immunsuppressives Mikroenvironment, indem sie PD1 exprimieren und damit die T-Zellen lahmlegen. Hier setzen die Immuncheckpointinhibitoren an: Die Hemmung von CTLA4 führt zur supraphysiologischen Aktivierung der T-Zellen, die Hemmung von PD1 erhält die T-Zell-Aktivität in der Umgebung des Tumors.
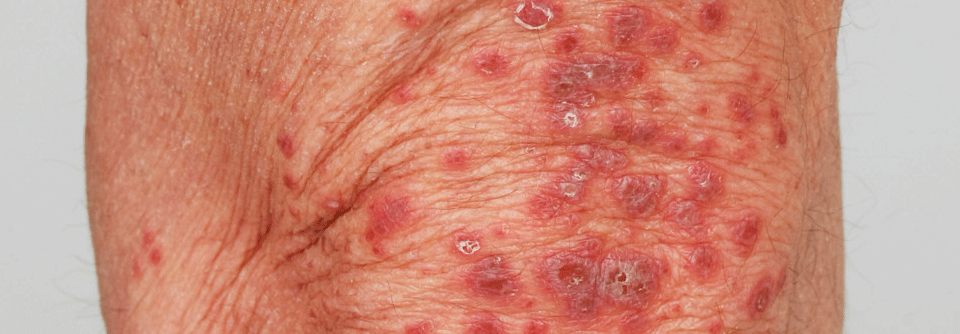
Die Kehrseite: Die Checkpointinhibition interferiert auch mit der Immuntoleranz, schwächt also den Schutz eigener Gewebe vor dem Immunsystem. Auch hier werden verschiedene Mechanismen verdächtigt. Aktivierte T-Zellen gehen z. B. gegen körpereigene Antigene vor, die den Tumorantigenen ähneln. So entstehen durch Checkpointhemmer induzierte Myokarditiden. Möglich ist auch, dass zusätzlich B-Zellen aktiviert und humorale Aktivität induziert wird, sodass Autoantikörper entstehen. Das ist etwa bei der Thyreoiditis der Fall, so die Expertin. Im Übermaß exprimierte Zytokine können Kolitiden induzieren.
Wieder andere Mechanismen greifen das Pankreas an. Dessen B-Zellen exprimieren PD-L1 und schützen sich so vor dem Angriff der T-Zellen. PD1-Antikörper zerstören diesen Schutzmechanismus. „Wir erleben unter diesen Medikamenten eine neue Form der massiven Betazelldestruktion samt Insulinmangeldiabetes“, berichtete Dr. Reger-Tan. Der Insulinmangel tritt sehr akut auf mit schweren Hyperglykämien und Ketoazidosen (60 % der Fälle bei Erstmanifestation).
Diabetes als Nebenwirkung unter Checkpointhemmern:
- Malignes Melanom
- Kopf-Hals-Tumoren
- Nicht-kleinzelliger Lungenkrebs
- Nierenzell- und Urothelkarzinom
- Hepatozelluläres und kolorektales Karzinom
- Hodgkin- und B-Zell-Lymphom
- Multiples Myelom
- Glioblastom
Diabeteserkrankung bleibt nicht nur vorübergehend
In einer Studie lag der mittlere Glukosespiegel bei über 650 mg/dl, das HbA1c bei knapp 8 %, bei den meisten Patienten war kaum noch C-Peptid nachweisbar. In etwa einem Drittel der Fälle waren auch Amylase und Lipase deutlich erhöht als Zeichen einer – asymptomatischen! – Pankreatitis. „Diese Fälle nehmen zu“, warnte die Diabetologin. Die Prävalenz liegt derzeit um 1 %, das heißt einer von 100 behandelten Patienten wird einen therapieinduzierten Typ-1-Diabetes entwickeln. Diese Nebenwirkung ist permanent, der Betroffene wird sein Leben lang Insulin brauchen. Wann sie eintritt, ist schwer vorherzusagen. „Es kann Tage dauern, aber auch mehrere Jahre“, so die Referentin. 70 % der Fälle ereigneten sich während der Behandlung, 10 % aber auch noch mehr als drei Monate nach Therapieende. Wichtig ist, sich nicht mit der Diabetesdiagnose zufriedenzugeben, sondern nach anderen immunvermittelten Nebenwirkungen zu suchen, betonte Dr. Reger-Tan. Diese sind vielfältig und umfassen auf endokrinologischer Seite u.a. Nebenniereninsuffizienz, Thyreoiditis und Hypophysitis, aber auch Organschäden wie Myokarditis, Hepatitis und Kolitis, die fulminant verlaufen können.Aufgepasst!
- nach einem Malignom in der Anamnese fragen und
- sich nach einer Therapie mit Immuncheckpointinhibitoren – vor allem PD1-Antikörpern – erkundigen.
Auf endokrine Störungen sollte gescreent werden
Hypophysitis und adrenale Insuffizienz sind klinisch oft schwer abgrenzbar gegen diabetische Ketoazidosen, warnte die Expertin. Sie gehen ebenso mit Übelkeit, Erbrechen und Vigilanzminderung einher bei niedrigem Insulinbedarf. Die Differenzierung sei lebenswichtig, denn Patienten mit Hypophysitis und Nebenniereninsuffizienz brauchen rasch hohe Dosen Hydrokortison. Die französische Fachgesellschaft für Endokrinologie hat Empfehlungen entwickelt, wie endokrine Nebenwirkungen von onkologischen Immuntherapien früh erkannt und behandelt werden sollten.1 Danach sollte jeder Patient vor und während der Therapie auf endokrine Störungen gescreent werden. Dazu gehören neben dem Nüchternblutzucker TSH und T4, Natriumspiegel, morgendliches Kortisol sowie die Sexualsteroide (LH, FSH, Testosteron/Estradiol). Im ersten halben Jahr sollten vor jedem Zyklus, danach alle zwei Zyklen die Messungen von Blutzucker, Schilddrüsenparametern, Natrium, Kortisol und bei Männern Testosteron wiederholt werden.Welche Punkte sollten beachtet werden?
Das Papier enthält außerdem einen Algorithmus, den Dr. Reger-Tan für den Umgang mit dem unter PD1-Antikörpern auftretenden Diabetes empfahl (unter Anti-CTLA4 kommen Diabetesfälle vor, aber wesentlich seltener, weshalb ein Screening nicht anzuraten ist):- Zunächst einmal sollten Patienten wissen, dass Typ-1-Diabetes und Ketoazidose auftreten können, und Symptome wie Gewichtsverlust, Polyurie und Polydipsie, Übelkeit und Erbrechen deuten lernen.
- Weckt die Klinik den Verdacht auf einen durch Checkpointhemmung verursachten Diabetes, sollten neben der üblichen Labordiagnostik mit Blutzucker und HbA1c auch Lipase und die wichtigsten Antikörper (Anti-GAD, falls negativ auch Anti-IA2 und -Znt8) gemessen werden. Eine Bildgebung des Pankreas liefert an diesem Punkt keine relevanten Zusatzinformationen.
- Bestätigt sich die Vermutung, muss unverzüglich die Insulintherapie eingeleitet werden und der Patient eine Schulung erhalten.
Quellen:
1. Castinetti F et al. Endocr Relat Cancer 2019; 26: G1-G18
Diabetes Kongress 2019