Nierenzellkarzinom: immer mehr Ablationsverfahren entwickelt
 Jeder zehnte kleine Nierentumor wird heute ablativ entfernt.
© iStock/Mohammed Haneefa Nizamudeen
Jeder zehnte kleine Nierentumor wird heute ablativ entfernt.
© iStock/Mohammed Haneefa Nizamudeen
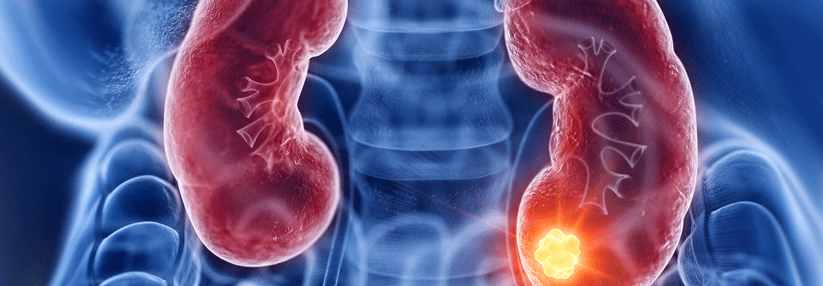
Nierenzellkarzinome gehören zu den zehn häufigsten Malignomen. Die Inzidenz steigt seit Jahren, weil die Menschen immer älter werden, vermehrt Schadstoffen ausgesetzt sind und Ärzte zunehmend auf die moderne bildgebende Diagnostik vertrauen. Im Frühstadium verursacht der Tumor in der Regel keine Symptome und stellt oft einen Zufallsbefund dar, schreiben Dr. Johann J. Wendler von der Universitätsklinik für Urologie Magdeburg und Kollegen.
Bei radiologisch typischen und malignomsuspekten Zeichen kann man von einem Nierenzellkarzinom ausgehen und hat damit die Indikation zur OP. Eine Biopsie braucht es nur, wenn sie die Wahl der Therapie beeinflusst. Leider fällt jede fünfte Probe falsch negativ oder nicht eindeutig aus, was eine erneute Entnahme nötig macht.
Als „kleines Karzinom“ gilt in Europa eine lokal begrenzte, nicht-metastasierte Raumforderung bis 4 cm Größe (T1a). Die Wachstums- und Absiedlungsrate nimmt allerdings bereits ab 3 cm exponentiell zu, betonen die Autoren. Ansonsten wies eine Reihe von Studien nach, dass T1a-Tumoren in den ersten fünf Jahren nur wenig zunehmen und kaum Filiae setzen. 20–30 % von ihnen entpuppen sich histologisch als gutartige Onkozytome.
Goldstandard der Therapie ist die Tumorenukleation, die das Nierenparenchym unbehelligt lässt und ohne Ischämie bzw. tiefgreifende Blutstillung auskommt. Bei der Enukleoresektion oder Organteilresektion dagegen entfernt man einen variablen Anteil an gesundem Gewebe mit und muss meistens das verbleibende Bett ausgedehnter versorgen.
Aus technischer Sicht ist jeder lokal begrenzte Befund operabel – aber nicht jeder Patient. Vor allem Alter und Komorbiditäten schränken hier ein. Während z.B. die Komplikationsrate von Nierenteilresektionen bei unter 50-Jährigen rund 30 % beträgt, klettert sie bei über 80-Jährigen auf bis zu 50 %. Kommen Begleiterkrankungen dazu, steigt sie auf das 6-Fache gegenüber „Gesunden“. Außerdem korreliert das Ausmaß von Kollateralschäden am Gewebe durch invasive Verfahren mit dem Risiko einer chronischen Niereninsuffizienz bzw. deren Verschlechterung.
Nun fällt der Höhepunkt der Nierenkrebs-Diagnosen ins siebte Lebensjahrzehnt. Dabei hat sich gezeigt, dass ein strukturiertes geriatrisches Assessment plus systematische Erfassung von Komorbiditäten in der Hälfte der Fälle zur Änderung des Therapiekonzeptes führt. Zudem fand man in zwei Studien an über 75-Jährigen keinen signifikanten Überlebensunterschied zwischen aktiver Überwachung (s. Kasten) und einer OP.
Die aktive Überwachung
Nonthermale Ablationstechniken in den Startlöchern
Radiofrequenzablation lässt sich wiederholen
Die perkutane Radiofrequenzablation ist zurzeit die am häufigsten eingesetzte Methode. In Analgosedierung appliziert man über Nadelelektroden hochfrequenten Wechselstrom. Es kommt dann zum alternierenden Ionenstrom und Reibungswärme, die letztlich in der Koagulationsnekrose mündet. Die Autoren empfehlen einen Sicherheitssaum von 5–10 mm mit zu versorgen. Die primäre Erfolgsrate liegt bei 90–100 %, Lokalrezidive treten bei 2–12 % der Patienten in den ersten fünf Jahren auf. Eine Radiofrequenzablation lässt sich jedoch wiederholen und schlägt dann fast zu 100 % an. Bei zentral gelegenen Tumoren mit direkter Beziehung zu Hilus und Beckenkelchsystem muss man allerdings mit inkompletten Ablationen rechnen. Und in der Nähe des Nierenbeckenkelchsystems und des Harnleiters raten die Autoren ganz von dem Verfahren ab, weil hier größere Gefahr für Perforationen oder die Bildung von Fisteln und Strikturen besteht.Quelle: Wendler JJ et al. Der Urologe 2018; 57: 731-743