Pankreaskrebs: Genetische Testung und Screening werden in Hochrisikokollektiven wichtiger
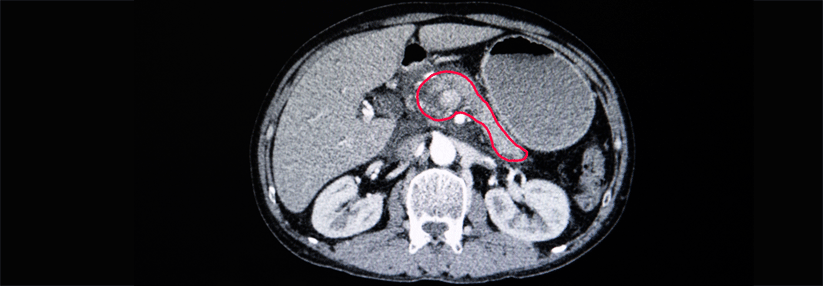
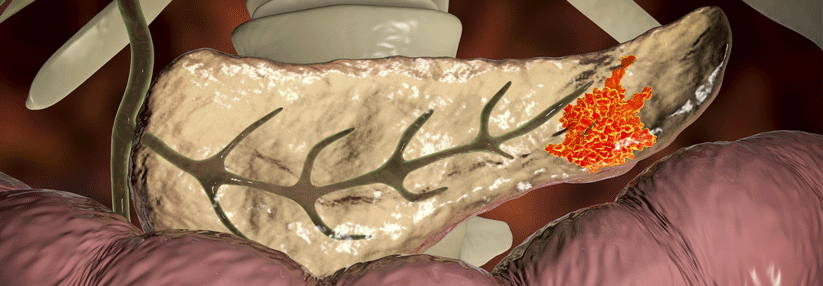
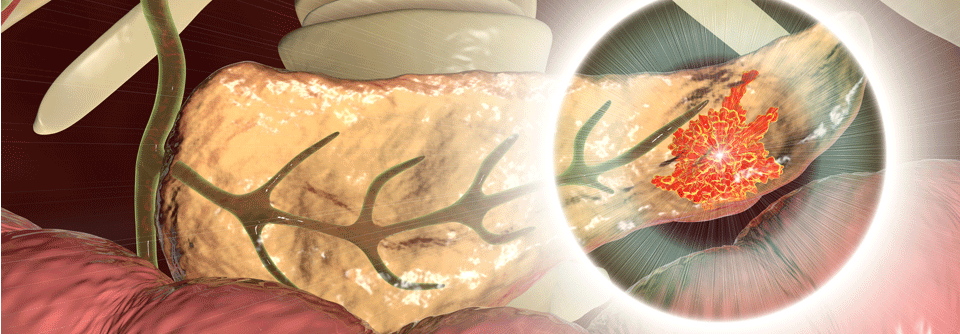
 Ab wann ein Screening durchgeführt werden sollte, wird durch den Mutationsstatus und die Familienanamnese bestimmt.
© iStock/AlexLMX, anusorn nakdee
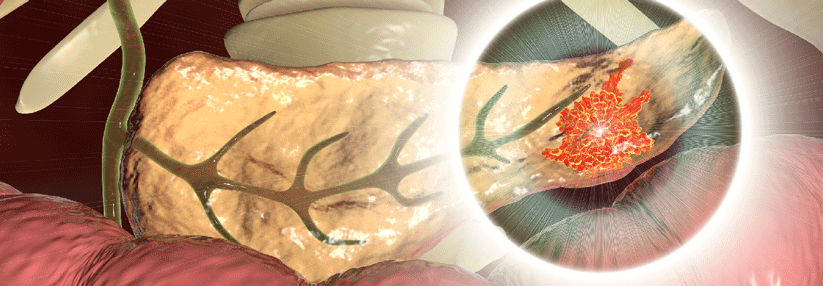
Ab wann ein Screening durchgeführt werden sollte, wird durch den Mutationsstatus und die Familienanamnese bestimmt.
© iStock/AlexLMX, anusorn nakdee
Neben Rauchen, Adipositas, Diabetes mellitus und Pankreatitis ist eine positive Familienanamnese ein wesentlicher Risikofaktor für die Entwicklung von Pankreaskarzinomen. „Bei etwa 10 % aller Patienten mit Pankreaskrebs lassen sich Keimbahnmutationen nachweisen“, berichtete Professor Dr. Sapna Syngal vom Dana-Farber Cancer Institute in Boston. Am häufigsten von Alterationen betroffen sind die Gene für BRCA1 und BRCA2, aber auch Mutationen in den ATM-, TP53- und PALB2-Genen kommen oft vor.
Aufgrund dieser Daten und der Entwicklung neuer Therapien für Patienten mit BRCA-mutierten Pankreaskarzinomen wird mitterweile, etwa von der American Society of Clinical Oncology (ASCO), direkt bei Diagnose eines Pankreaskarzinoms die genetische Testung gefordert. Die Leitlinien des National Comprehensive Cancer Network (NCCN) sprechen sich bei Personen mit Pankreaskrebs und positiver Familienanamnese für die Testung aus.
Wegen der großen Heterogenität der genetischen Anomalien sollte die Testung mit einem Multigen-Panel durchgeführt werden, das alle bekannten Alterationen umfasst, betonte Prof. Syngal. Allerdings sind die Testraten bislang noch niedrig. Als wichtig bezeichnete die Referentin daher die Implementierung eines Überweisungssystems in onkologischen Praxen und die automatische Erfassung von diagnostizierten Betroffenen.
Testraten steigen auf knapp 40 %
Nach Etablierung dieser Maßnahmen im Rahmen von Studien gelang ein Anstieg der Testraten von zunächst nur 8 % auf mittlerweile 37 %. Prof. Syngal geht davon aus, dass neue Daten zur zielgerichteten Therapie beim Pankreaskarzinom in dieser Hinsicht weitere Fortschritte bringen werden.
Eckdaten zum Screening
- alle Patienten mit Peutz-Jeghers-Syndrom (STK11-Mutation),
- Träger der CDKN2A-Mutation,
- Träger der Keimbahnmutationen BRCA1/2, PALB2, ATM, MLH1, MSH2 und MSH6 mit mindestens einem betroffenen Verwandten ersten Grades sowie
- Personen mit mindestens einem betroffenen Verwandten ersten Grades, bei dem ebenfalls ein Verwandter ersten Grades an Pankreaskrebs erkrankt ist.
* The Cancer of the Pancreas Screening
Quellen:
1. Goggins M et al. Gut 2020; 69: 7-17; DOI: 10.1136/gutjnl-2019-319352
Syngal S et al. ASCO-GI 2020; „Breakout: Risk Reduction in Hereditary Cancers and High-Risk Groups“