HPV-assoziierte Oropharynxkarzinome: Rezidivrisiko im Blut bestimmen
 In der Studie wurde nach den fünf häufigsten Hochrisiko-Typen der humanen Papillomviren gescreent. Das sind Typ 16, 18, 31, 33 und 35.
© iStock/xrender
In der Studie wurde nach den fünf häufigsten Hochrisiko-Typen der humanen Papillomviren gescreent. Das sind Typ 16, 18, 31, 33 und 35.
© iStock/xrender
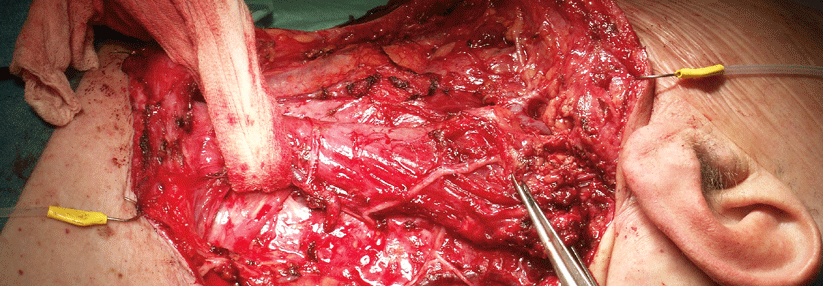
Das Plattenepithelkarzinom des Oropharynx (OPSCC) ist in den letzten zehn Jahren zum häufigsten mit humanen Papillomviren (HPV) assoziierten Tumor geworden. Die Prognose dieses Tumortyps ist besser als die von HPV-negativen OPSCC. Deshalb wird versucht, die Therapie weniger intensiv zu gestalten, ohne die Heilungsaussichten zu beeinträchtigen. Eine Möglichkeit könnte die regelmäßige Suche nach DNA der HP-Viren im Blut sein, die im positiven Fall eventuell ein Rezidiv vorhersagen könnten, schreiben Wissenschaftler der University of North Carolina in Chapel Hill.
Zu diesem Zweck wurde in einer prospektiven Studie mit 115 Patienten mit HPV-positivem OPSCC untersucht, ob man die Bestimmung der…
Bitte geben Sie Ihren Benutzernamen und Ihr Passwort ein, um sich an der Website anzumelden.