Todeskandidatin geheilt: Kultivierte T-Zell-Spezialisten ließen Brustkrebsmetastasen verschwinden
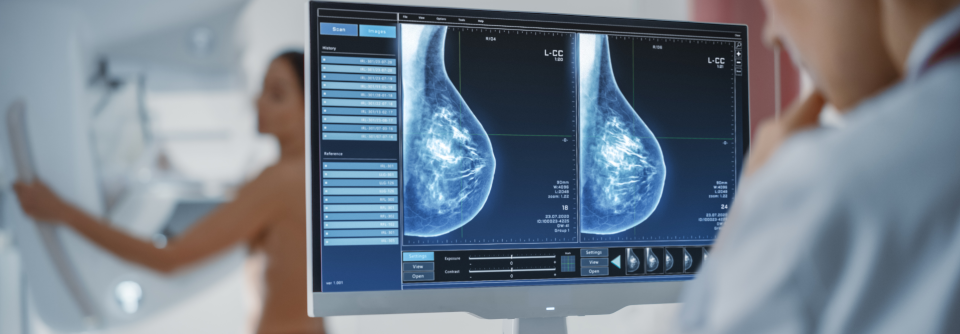
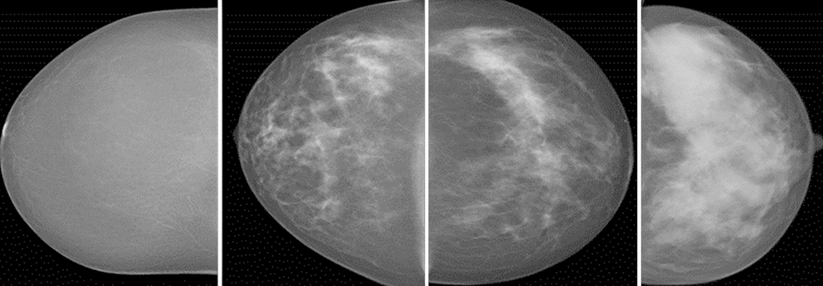
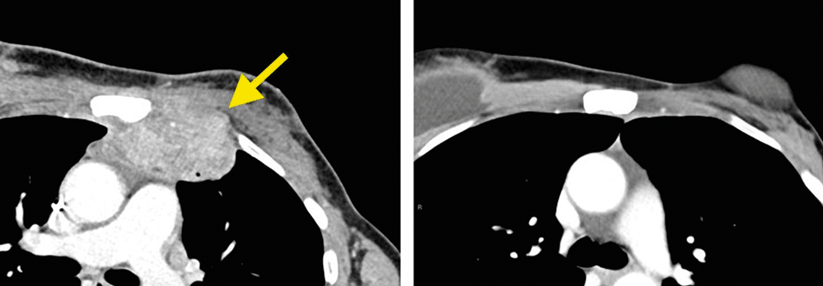 Im CT der Patientin sind die Filiae in der Brustwand (links) deutlich zu erkennen. 14 Monate nach der speziellen adoptiven Immuntherapie ist der CT-Befund unauffällig (rechts).
© National Cancer Institute
Im CT der Patientin sind die Filiae in der Brustwand (links) deutlich zu erkennen. 14 Monate nach der speziellen adoptiven Immuntherapie ist der CT-Befund unauffällig (rechts).
© National Cancer Institute
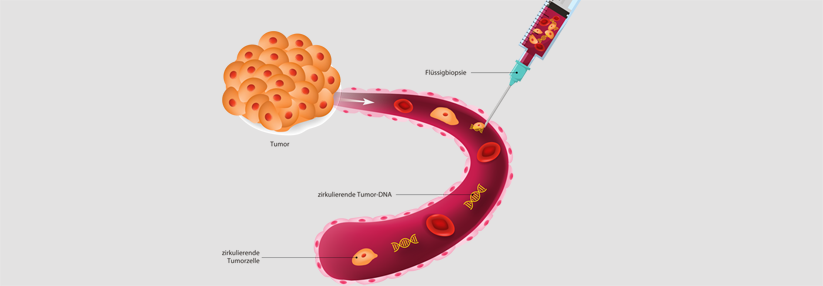
Für den adoptiven Zelltransfer entnimmt man dem krebskranken Patienten T-Lymphozyten aus Blut, Knochenmark oder Tumorgewebe und kultiviert sie in-vitro. Tumorspezifische T-Zellen werden dabei selektiv vermehrt oder gentechnisch so verändert, dass sie bestimmte Tumorantigene erkennen können. Über eine Infusion erhält der Patient die Zellen anschließend zurück. Die hohe Zahl spezialisierter zytotoxischer T-Zellen führt zu einer krebsspezifischen Immunreaktion. Um den Effekt zu verstärken, kann vorher chemotherapeutisch eine Lymphozytendepletion erfolgen.
Bei mutationsreichen Krebsarten wie Melanomen konnte man das Verfahren schon mit Erfolg einsetzen, schreiben Dr. Nikolaos Zacharakis vom US National Cancer Institute in Bethesda und Kollegen. Die Therapie epithelialer Tumoren mit nur wenigen Mutationen, beispielsweise Brust- oder Magenkrebs, war dagegen bislang kaum effektiv.
Die Wissenschaftler haben deshalb die ursprüngliche Methode des adoptiven Zelltransfers weiterentwickelt und bei einer 49-Jährigen mit rezidiviertem, metastasiertem und therapieresistentem Brustkrebs getestet.
Kombinationstherapie mit Checkpoint-Inhibitor
Durch Exom-* und RNA-Sequenzierung von Metastasen- und gesundem Gewebe der Patientin konnten die Forscher zunächst 62 für den Krebs spezifische Mutationen identifizieren. Im Pool der aus Tumorgewebe gewonnenen T-Lymphozyten identifizierten sie dann jene Zellen, die Proteine erkannten, die anhand der mutierten Gene entstanden sind. Für die Therapie wählten sie schließlich elf T-Zell-Klone aus, die spezifisch auf vier verschiedene dieser Krebsantigene zielten und vermehrten diese unter Zusatz von Interleukin-2, einem T-Zell-Wachstumsfaktor.
Eine Woche vor der Zellinfusion begannen die Kollegen vom National Cancer Institute bei ihrer Patientin mit der vorbereitenden Lymphozytendepletion. Die Begleittherapie mit Pembrozilumab, einem Immun-Checkpoint-Inhibitor, wurde zwei Tage vor der Infusion gestartet und neun Wochen lang weitergeführt. Zusätzlich zur Applikation der tumorinfiltrierenden Lymphozyten bekam die Frau Interleukin-2.
Nach einem Jahr keine Tumoren mehr zu sehen
Sechs Wochen nach der Zellinfusion war die Tumorlast um 51 % zurückgegangen, nach einem Jahr konnten in der Bildgebung keine Läsionen mehr nachgewiesen werden. Weitere zwölf Monate später hatte sich an diesem positiven Ergebnis nichts geändert. Acht der elf infundierten T-Zell-Klone ließen sich 17 Monate nach der Behandlung noch im Blut der Patientin nachweisen, was auf eine dauerhafte Immunantwort hindeutet.
Wie die Autoren aus eigener Studienerfahrung berichten, scheint ihre Therapiemethode auch für Patienten mit Leber- oder Dickdarmkrebs geeignet zu sein.
* Das Exom enthält im Gegensatz zum Genom nur die kodierenden DNA-Abschnitte. Bei der Standard-Exomsequenzierung werden etwa 20 000 Gene sequenziert (etwa 50 Millionen Basen)
Quelle: Zacharakis N et al. Nat Med 2018; 24: 724-730
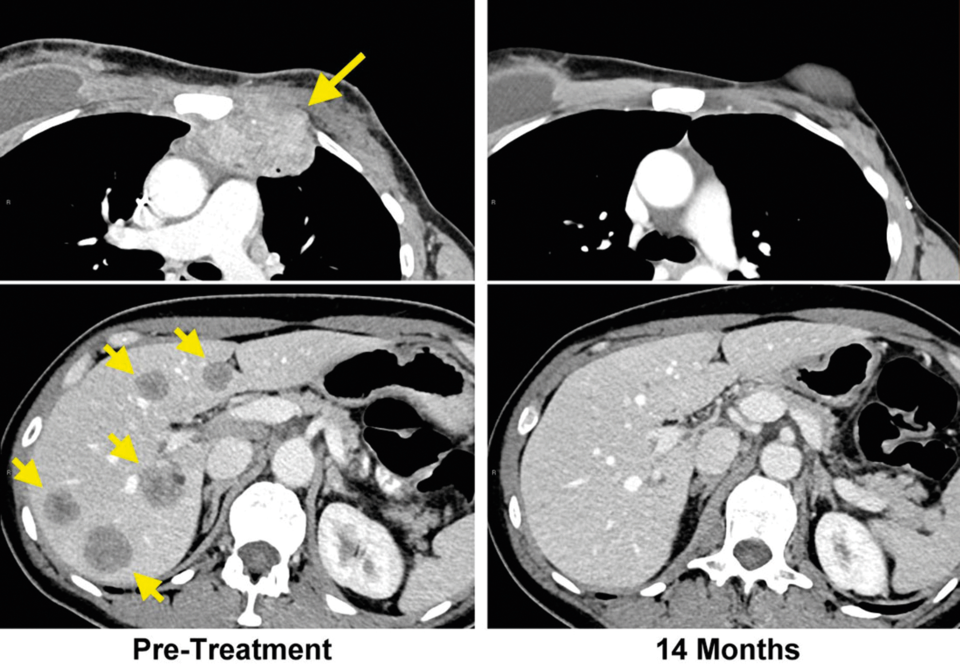 Im CT der Patientin mit chemotherapieresistentem, metastasiertem Brustkrebs sind die Filiae in Brustwand (links oben) und Leber (links unten) deutlich zu erkennen. 14 Monate nach der speziellen adoptiven Immuntherapie ist der CT-Befund unauffällig (rechts oben, rechts unten).
© National Cancer Institute
Im CT der Patientin mit chemotherapieresistentem, metastasiertem Brustkrebs sind die Filiae in Brustwand (links oben) und Leber (links unten) deutlich zu erkennen. 14 Monate nach der speziellen adoptiven Immuntherapie ist der CT-Befund unauffällig (rechts oben, rechts unten).
© National Cancer Institute
Verwandte Links
- Breast cancer patient benefits from modified immunotherapy Zacharakis N et al. Nat Med 2018; 24: 724-730
Bereiche
- Allergologie
- Allgemeinmedizin
- Alternativmedizin
- Angiologie
- Chirurgie
- Dermatologie
- Diabetologie
- Endokrinologie
- Gastroenterologie
- Geriatrie
- Gynäkologie
- HNO
- Infektiologie
- Innere Medizin
- Kardiologie
- Naturheilkunde
- Nephrologie
- Neurologie
- Onkologie und Hämatologie
- Ophthalmologie
- Orthopädie
- Pädiatrie
- Palliativmedizin und Schmerzmedizin
- Pneumologie
- Psychiatrie
- Rheumatologie
- Sportmedizin
- Urologie
- Alle Beiträge
- Kongress aktuell